Теория:
Степень окисления радона (Rn) в подавляющем большинстве случаев принимает значение 0.
Как благородный газ, он обладает завершенной электронной оболочкой, что делает его химически крайне инертным.
Однако, будучи самым тяжелым из природных инертных газов, радон способен вступать во взаимодействия с сильнейшими окислителями, проявляя положительные значения +2, +4 и +6.
Показатель 0 относится к радону в его стандартном состоянии (одноатомный бесцветный газ без запаха).
Например для наиболее стабильной формы: в свободном виде как газ Rn заряд атома равен 0. В таком состоянии он практически не реагирует с другими веществами.
Для сравнения, СО +2: теоретически предсказана и экспериментально подтверждена в таких нестабильных соединениях, как RnF2 (дифторид радона). В этой форме радон отдает два своих электрона наиболее электроотрицательному элементу — фтору.
- Почему 0? У радона полностью заполнены внешние энергетические уровни (6s2 6p6). Такая конфигурация энергетически очень выгодна, и атому «невыгодно» нарушать эту симметрию.
- Почему возможны положительные СО? Радон — массивный атом. Его внешние электроны находятся далеко от ядра и прикрыты внутренними слоями, поэтому мощные окислители могут «вырвать» их, переводя элемент в состояния +2 или выше.
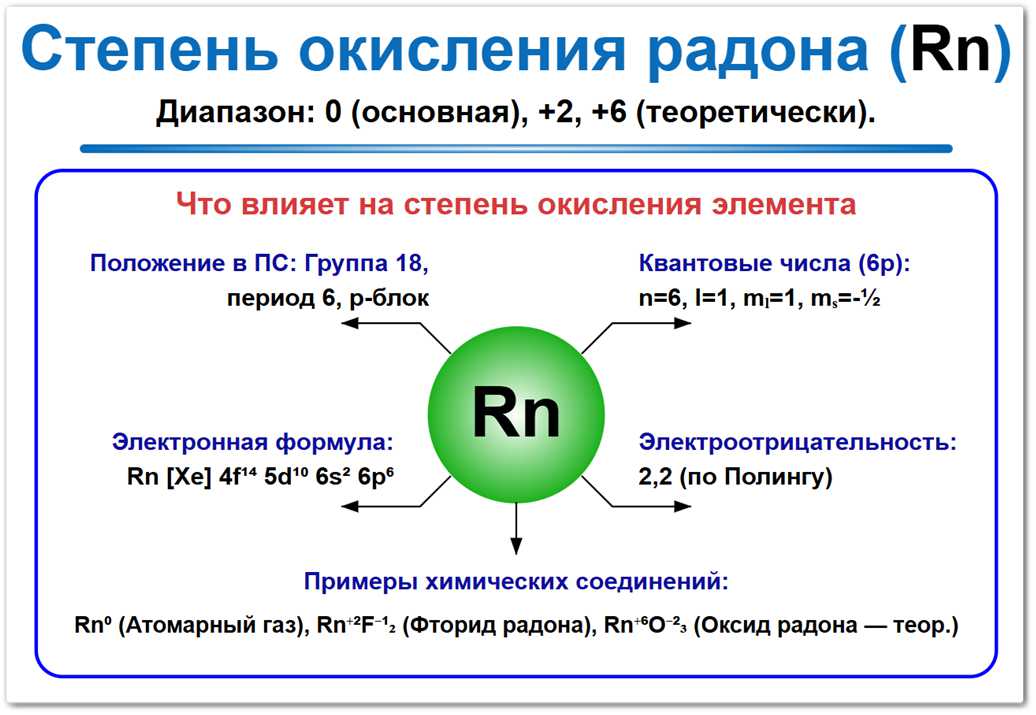
Рис. 1. Возможные степени окисления радона: от 0 до +6.
Состояние 0 является единственно устойчивым в естественных условиях, в то время как фториды радона крайне нестабильны и склонны к разложению.
Важно помнить, что радон — это радиоактивный газ.
Его изучение осложняется не только химической инертностью, но и коротким периодом полураспада изотопов, что делает создание стабильных химических связей практически невозможным.
На свойства этого элемента влияют завершенное электронное строение (4f14 5d10 6s2 6p6), высокий потенциал ионизации и значение электроотрицательности по разным шкалам (около 2,2 по Полингу, расчетно).
Содержание страницы
- 1. Почему 0 — основная степень окисления у радона
- 2. Степень окисления радона в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему радон почти всегда сохраняет заряд 0?
- 4. 4 способа определить степень окисления радона
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления радона
- 6. Шпаргалка для радона
- 7. Радон вне учебника: какие степени окисления обсуждают ученые?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему 0 — основная степень окисления у радона
Причина стабильности нулевого состояния заключается в правиле октета: наличие 8 электронов на внешнем уровне обеспечивает химическую пассивность.
- В свободном атоме (Rn0): Заряд равен 0. Электронная формула:
[Xe] 4f14 5d10 6s2 6p6. - В дифториде (Rn+2): Радон формально отдает 2 электрона фтору. Конфигурация:
[Xe] 4f14 5d10 6s2 6p4.

Рис. 2. Схема внешний слой (6s2 6p6) полностью завершен. Газ химически инертен.
Степень окисления радона в соединениях
Хотя химия этого газа изучена слабо из-за радиации, радон в соединениях проявляет степень окисления в следующих гипотетических и синтезированных структурах:
- Дифторид радона (RnF2): Rn +2.
- Тетрафторид радона (RnF4): Rn +4 (предсказано теоретически).
- Триоксид радона (RnO3): Rn +6 (теоретическая модель).
- Клатраты радона (Rn·6H2O): Rn 0 (связи удерживаются силами Ван-дер-Ваальса).
- Фторсульфат радона (Rn(OSO2F)2): Rn +2.
Высшая степень окисления
Высшая степень окисления Rn теоретически может достигать +6. В этом состоянии он мог бы образовывать оксиды, подобные ксенону, но такие вещества крайне взрывоопасны и нестабильны.
Низшая степень окисления
Для радона характерна степень окисления 0. Поскольку он является неметаллом с высокой энергией ионизации, отрицательные значения для него не зафиксированы.
Промежуточные степени окисления
Степень окисления радона в веществах со значением +4 считается возможной в среде суперкислот или при сверхвысоких давлениях фтора, однако экспериментальные данные остаются крайне скудными.
Важно: Радон — самый химически активный среди инертных газов (не считая искусственно полученного оганесона). Его степень окисления радона формула соединения всегда будет положительной только в паре с самыми агрессивными неметаллами.
Почему радон почти всегда сохраняет заряд 0?
Характер поведения элемента продиктован его нахождением в 18-й группе:
- Нейтральная СО (0): Атом самодостаточен. Ему не нужно отдавать или принимать электроны для стабильности.
- Положительная СО (+): Возникает только под давлением фтора. Электроны уходят с внешнего p-подуровня.
- Отсутствие отрицательных СО (-): Радону некуда принимать дополнительные электроны, так как текущий уровень полностью укомплектован.
4 способа определить степень окисления радона
По таблице Менделеева
- Семейство: p-элемент (благородные газы).
- Валентные электроны: 8 электронов (6s2 6p6).
- Атомная масса радона: [222] а.е.м. (наиболее стабильный изотоп).
По валентности (Число связей)
В обычных условиях валентность радона равна 0, но может достигать II, IV или VI.
- В свободном виде: Не образует связей, СО — 0.
- В RnF2: Образует две ковалентные связи, СО — +2.
По электронной конфигурации
- Электронная формула радона: [Xe] 4f14 5d10 6s2 6p6.
- Атому радона степени окисления +2 достичь сложнее, чем ксенону, но легче, чем криптону, из-за увеличения радиуса атома.
По химическому соединению (Алгебраический расчет)
Пример для RnF2:
Сумма СО равна 0. Фтор всегда -1. Обозначим радон как x.
x + 2 · (-1) = 0 ⇒ x — 2 = 0 ⇒ x = +2
Примеры степеней окисления радона
| СО | Характеристика | Примеры соединений |
|---|---|---|
| 0 | Стандартная. Единственная форма существования в природе. | Rn (газ) |
| +2 | Экспериментальная. Получена в реакциях с фтором. | RnF2 |
| +6 | Теоретическая. Предсказана для оксидов, но не выделена. | RnO3 (гипотетически) |
Шпаргалка для радона
- 0 — подавляющая степень окисления, газ химически пассивен.
- Радиоактивность — главная черта; радон распадается быстрее, чем успевает прореагировать.
- Фториды — единственные подтвержденные химические соединения радона.
Радон вне учебника: какие степени окисления обсуждают ученые?
+8: В отличие от ксенона, для радона состояние +8 считается практически недостижимым из-за релятивистской стабилизации 6s-электронов.
Клатраты (СО 0): Радон может застревать в «клетках» из молекул воды или хинона. Там его заряд остается нулевым, так как химическая связь не образуется.
Ионные формы: В растворах сильных кислот радон может вести себя как катион (например, RnF⁺), что формально оставляет его в степени +2.
Пример решения задачи:
▶️ Дано:
Соединение: RnF2 (дифторид радона).
⌕ Найти:
Определите СО радона.
✨ Решение:
Фтор (F) — самый сильный окислитель с постоянной СО -1. Уравнение: x + 2 · (-1) = 0. Отсюда x = 2.
✅ Ответ:
Rn(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3.
Разбор ошибок:
3 — верно: чем больше радиус атома инертного газа, тем легче его окислить.
4 — неверно: благородные газы не проявляют отрицательных СО.
Часто задаваемые вопросы
Самой стабильной степенью окисления считается +2.
Он самый тяжелый из стабильных представителей своей группы (не считая искусственного оганесона).
Из-за большого радиуса атома его внешние электроны удерживаются слабее, чем у ксенона, что позволяет ему вступать в химические реакции.
Да, как и у других элементов 18-й группы, его электроотрицательность не позволяет захватывать чужие электроны.
Всё дело в размере атома и расстоянии до ядра. Хотя радон (Rn) — благородный газ с заполненной электронной оболочкой (6s2 6p6), он находится в самом низу таблицы Менделеева.
Это делает его особенным:
1. Слабая хватка ядра.
2. Низкий потенциал ионизации.
3. Металлический характер.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.