Теория:
Степень окисления плутония (Pu) в химических соединениях отличается исключительным разнообразием, принимая значения +3, +4, +5, +6 и иногда +7.
Это обусловлено сложным строением электронной оболочки и близостью энергетических уровней 5f, 6d и 7s орбиталей, что позволяет атому легко варьировать число отдаваемых электронов.
Кроме того, выделяют показатель 0, который относится к плутонию в виде простого вещества (плотный, радиоактивный серебристый металл, меняющий свою плотность при фазовых переходах).
Например для одной из важнейших СО +4: в соединении PuO2 (диоксид плутония) или PuF4 (тетрафторид плутония) заряд иона равен +4.
В этом состоянии плутоний проявляет химическое сходство с торием и ураном.
Для сравнения, СО +6: проявляется в таких веществах, как PuF6 (гексафторид плутония) или в ионе плутонила PuO22+. Здесь он ведет себя подобно урану в высшей степени окисления.
- Почему так много степеней? Плутоний — актиноид, у которого 5f-электроны еще не стали окончательно «инертными» (как у лантаноидов), поэтому они активно участвуют в создании химических связей.
- Почему +4 наиболее стабильна в твердом теле? В кристаллической решетке диоксида плутония состояние +4 энергетически выгодно, что делает этот материал идеальным топливом для ядерных реакторов.
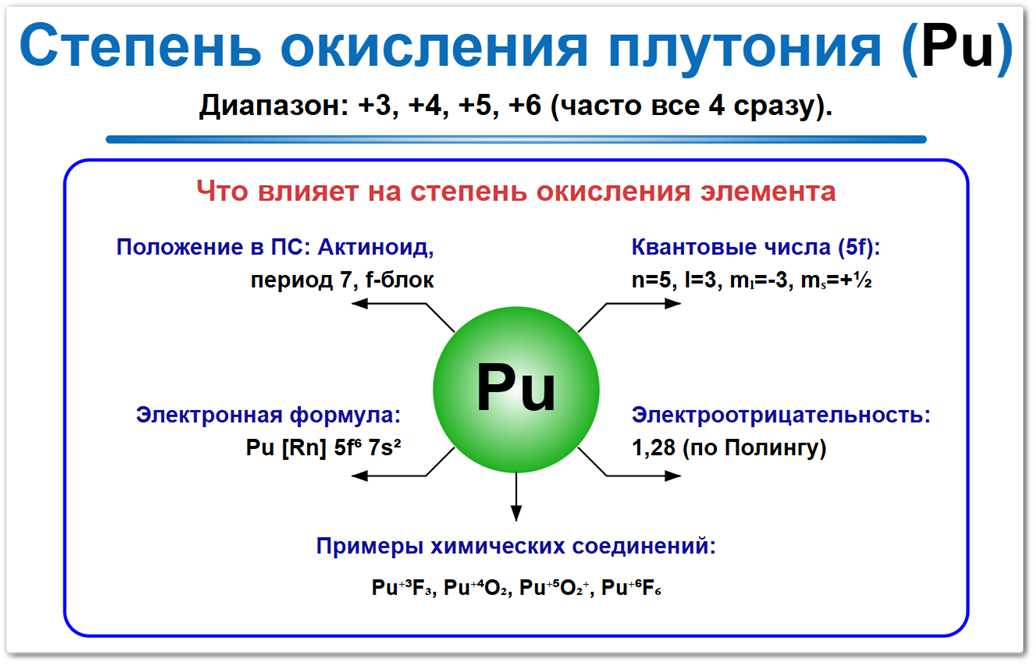
Рис. 1. Основные степени окисления плутония: +3, +4, +5, +6 и +7.
Интересно, что в водных растворах плутоний может одновременно существовать в нескольких степенях окисления (+3, +4, +5, +6).
Окрашивая жидкость в различные цвета (от синего до розового и зеленого).
Важно помнить, что плутоний крайне токсичен и радиоактивен, что делает его изучение делом высокой опасности и требует сложной защиты.
На свойства этого актиноида влияют электронное строение (5f6 7s2), актиноидное сжатие и значение электроотрицательности 1,28 по шкале Полинга.
Содержание страницы
- 1. Почему +4 — самая характерная степень окисления у плутония
- 2. Степень окисления плутония в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему плутоний предпочитает заряды +3, +4, +5 и +6?
- 4. 4 способа определить степень окисления плутония
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления плутония
- 6. Шпаргалка для плутония
- 7. Плутоний вне учебника: какие степени окисления существуют только в теории или крайне сложны?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +4 — самая характерная степень окисления у плутония
Причина преобладания четырехвалентного состояния кроется в оптимальном балансе между энергией ионизации и стабильностью образующихся комплексов.
- В простом веществе (Pu0): Заряд равен 0. Конфигурация:
[Rn] 5f6 7s2. - В четырехвалентном ионе (Pu+4): Плутоний теряет 4 электрона, образуя устойчивый катион.
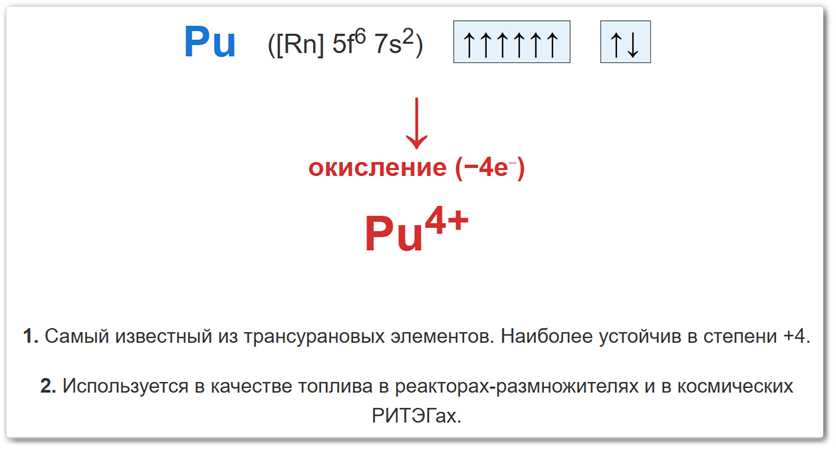
Рис. 2. Схема образования степени окисления +4: удаление двух электронов с 7s-орбитали и двух — с 5f-подуровня.
Степень окисления плутония в соединениях
В зависимости от условий среды, плутоний в соединениях проявляет степень окисления, определяющую его реакционную способность:
- Диоксид плутония (PuO2): Pu +4.
- Нитрат плутония(IV) (Pu(NO3)4): Pu +4.
- Гексафторид плутония (PuF6): Pu +6 (летучее вещество).
- Гидрид плутония (PuH3): Pu +3.
- Перплутонат калия (KPuO5): Pu +7.
Высшая степень окисления
Высшая степень окисления Pu равна +7. Она достигается в сильнощелочных растворах при мощном окислении.
Это крайне агрессивная форма, быстро восстанавливающаяся до +6.
Низшая степень окисления
Для плутония типична степень окисления 0 в металлическом виде. В химических соединениях низшим стабильным состоянием является +3.
Промежуточные степени окисления
Степень окисления плутония в веществах часто принимает значения +5. Например, в ионах PuO2+ (плутонил-ион), которые важны в геохимии и экологии.
Важно: Плутоний — настоящий мастер «маскировки». Из-за способности легко переходить из одной степени окисления в другую, его крайне сложно полностью удалить из химических отходов, так как он постоянно меняет свое поведение.
Почему плутоний предпочитает заряды +3, +4, +5 и +6?
Характер поведения продиктован его местом в 7-м периоде (актиноиды):
- Положительная СО (+): Атом плутония легко отдает электроны. Большое число возможных степеней окисления связано с тем, что 5f-электроны слабо экранированы.
- Отсутствие отрицательных СО (-): Как и все металлы, плутоний имеет очень низкую электроотрицательность и не склонен принимать лишние электроны.
4 способа определить степень окисления плутония
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 8 электронов (5f6 7s2).
- Атомная масса плутония: 244 а.е.м.
По валентности (Число связей)
Обычно валентность плутония может быть III, IV, V или VI.
- В PuO2: Плутоний образует четыре связи с кислородом, СО — +4.
- В PuF6: Плутоний образует шесть связей, СО — +6.
По электронной конфигурации
- Электронная формула плутония: [Rn] 5f6 7s2.
- Атому плутония степени окисления +4 достичь наиболее просто, так как это создает энергетически сбалансированную структуру.
По химическому соединению (Алгебраический расчет)
Пример для PuF6:
Сумма СО равна 0. Фтор всегда -1. Обозначим плутоний как x.
x + 6 · (-1) = 0 ⇒ x — 6 = 0 ⇒ x = +6
Примеры степеней окисления плутония
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Наиболее стабильная. Основа ядерного топлива (оксид). | PuO2, PuF4 |
| +3, +6 | Реакционноспособные. Легко переходят в +4. | PuCl3, PuF6 |
| 0 | Металл. Сложное простое вещество с 6 фазами. | Pu (металл) |
Шпаргалка для плутония
- +4 — «золотая середина», самая предсказуемая степень окисления.
- +7 — проявляется только в экстремально щелочной среде.
- Радиохимическое поведение — плутоний «любит» менять заряд, что осложняет его переработку.
Плутоний вне учебника: какие степени окисления существуют только в теории или крайне сложны?
+2: В стандартных условиях не существует. Однако в специфических металлоорганических соединениях (комплексах с «объемными» лигандами) ученым удалось синтезировать производные плутония (II).
Это требует работы при сверхнизких температурах и инертной атмосфере.
Теоретические пределы: Выше +7 плутоний подняться не может, так как для этого потребовалось бы отдать электроны из заполненных глубоких уровней, что энергетически невозможно.
Интересный факт: Плутоний — один из немногих элементов, способных находиться в растворе в четырех разных степенях окисления одновременно (+3, +4, +5, +6). Этот «цветной хоровод» делает его уникальным объектом для изучения квантовой химии и спектроскопии.
Пример решения задачи:
▶️ Дано:
Соединение: PuF4 (тетрафторид плутония).
⌕ Найти:
Определите СО плутония.
✨ Решение:
Фтор имеет заряд -1. В молекуле 4 атома фтора (суммарно -4). Чтобы молекула была нейтральна, заряд плутония равен +4.
✅ Ответ:
Pu(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: в диоксиде (PuO2) степень окисления плутония равна +4 (2 атома кислорода по -2 дают -4).
Часто задаваемые вопросы
Для твердых соединений — СО +4, для растворов — зависит от кислотности среды.
Это металл с низкой электроотрицательностью; он «запрограммирован» отдавать электроны для формирования связей.
У него много степеней окисления (от +2 до +7) из-за особенностей строения его атома:
Энергетическая близость уровней: Электроны на 5f и 6d орбиталях обладают близкими энергиями. Это позволяет атому легко «отдавать» разное количество электронов, не тратя на это критически много энергии.
Экранирование: 5f-электроны слабо экранированы от ядра, что делает их химически активными и позволяет им участвовать в образовании связей, обеспечивая вариативность состояний.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.