Теория:
Степень окисления калифорния (Cf) в химических соединениях чаще всего принимает значение +3.
Это состояние обусловлено конфигурацией 5f-орбиталей, которые у тяжелых актиноидов становятся всё более стабильными и «закрытыми», подобно 4f-электронам лантаноидов.
5f‑орбитали калифорния всё же могут участвовать в связывании, хотя и в меньшей степени.
Способен проявлять и другие степени окисления:
+2 — встречается реже и считается менее устойчивой по сравнению с +3, но не является «крайне нестабильной»: существуют экспериментально подтверждённые соединения, например дииодид калифорния CfI2.
+4 — также реализуется на практике, вопреки утверждению о чисто теоретическом существовании. Примером служит диоксид калифорния CfO2.
Помимо этого, выделяют показатель 0, относящийся к калифорнию в виде простого вещества (серебристый, достаточно мягкий переходный металл).
Например для наиболее стабильной СО +3: в соединении CfCl3 (хлорид калифорния III) или Cf2O3 (оксид калифорния III) заряд иона равен +3.
В этом состоянии калифорний крайне похож на диспрозий — своего «двойника» из семейства редкоземельных элементов.
Для сравнения, редкая СО +2: проявляется при восстановлении трихлорида калифорния металлическим калием в расплаве.
В таких условиях можно получить соединения типа CfCl2, однако они крайне неустойчивы и стремятся окислиться.
- Почему +3? Атом калифорния легко отдает три внешних электрона (два с 7s и один с 5f или 6d), достигая устойчивой электронной конфигурации.
- Почему другие состояния нестабильны? Энергия связи 5f-электронов у калифорния уже достаточно велика, поэтому их вовлечение в химическую связь (для получения СО +4 и выше) требует экстремальных условий или специфических лигандов.
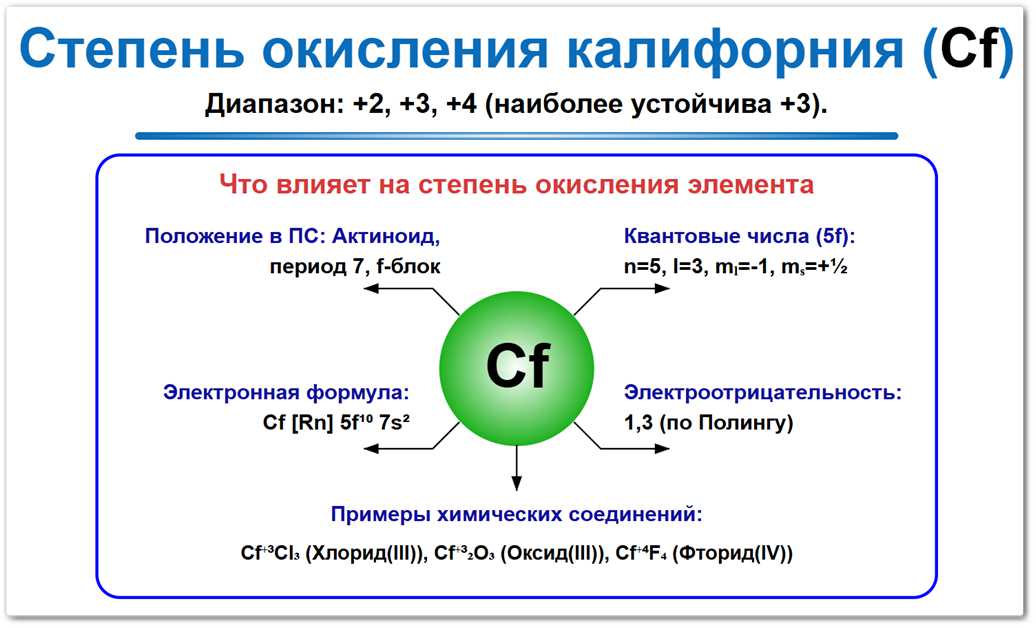
Рис. 1. Основные степени окисления калифорния: 0, +2 и +3.
Состояние +3 является доминирующим в любых водных растворах. Калифорний — это искусственно синтезированный радиоактивный элемент, чья химия изучается в микроколичествах.
Важно отметить, что все соединения калифорния обладают высокой альфа-радиоактивностью, что усложняет их химический анализ.
На его свойства влияют электронное строение (5f10 7s2), актиноидное сжатие и крайне низкая электроотрицательность.
Содержание страницы
- 1. Почему +3 — самая устойчивая степень окисления у калифорния
- 2. Степень окисления калифорния в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему калифорний выбирает преимущественно заряд +3?
- 4. 4 способа определить степень окисления калифорния
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления калифорния
- 6. Шпаргалка для калифорния
- 7. Калифорний вне учебника: существуют ли иные состояния?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +3 — самая устойчивая степень окисления у калифорния
Стабильность этой формы объясняется достижением энергетически выгодной электронной конфигурации, при которой оставшиеся f-электроны прочно удерживаются ядром.
- В простом веществе (Cf0): Заряд равен 0. Конфигурация:
[Rn] 5f10 7s2. - В трехвалентном ионе (Cf+3): Калифорний отдает электроны с 7s и 5f подуровней. Конфигурация:
[Rn] 5f9.
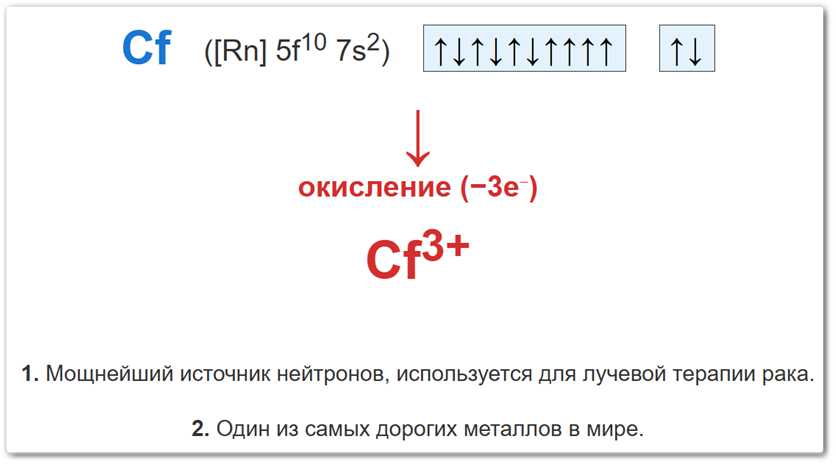
Рис. 2. Схема образования степени окисления +3: переход нейтрального атома в катион 3+.
Степень окисления калифорния в соединениях
В специфических лабораторных условиях калифорний в соединениях проявляет степень окисления, зависящую от метода синтеза:
- Трихлорид калифорния (CfCl3): Cf +3.
- Оксид калифорния (Cf2O3): Cf +3.
- Дихлорид калифорния (CfCl2): Cf +2 (получен в расплавах).
- Оксифторид калифорния (CfOF): Cf +3.
Высшая степень окисления
Высшая степень окисления Cf равна +3. В этом состоянии он ведет себя как типичный лантаноид, образуя прочные координационные соединения.
Низшая степень окисления
Для калифорния характерна степень окисления 0 в металлической фазе. Отрицательные значения для него невозможны из-за ярко выраженного металлического характера.
Промежуточные степени окисления
Степень окисления калифорния в веществах изредка может принимать значение +2 (в галогенидах), однако такие соединения крайне склонны к окислению до +3 при контакте даже с микроскопическими следами воды или кислорода.
Важно: Калифорний часто называют «тяжелым аналогом диспрозия», так как их ионные радиусы и химическое поведение в степени +3 практически идентичны, что является следствием актиноидного сжатия.
Почему калифорний выбирает преимущественно заряд +3?
Химическая природа элемента предопределена его положением в конце ряда актиноидов:
- Положительная СО (+): Атом активно отдает электроны. Уровни 5f становятся слишком глубокими, чтобы их можно было легко изменять, поэтому +3 становится «тупиковой» и максимально стабильной точкой.
- Отсутствие отрицательных СО (-): Как и все радиоактивные металлы этой группы, калифорний обладает крайне низкой электроотрицательностью и не способен удерживать дополнительные электроны.
4 способа определить степень окисления калифорния
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 2 электрона на 7s (и 10 на 5f).
- Атомная масса калифорния: ~251 а.е.м.
По валентности (Число связей)
Обычно валентность калифорния соответствует значению III.
- В CfCl3: Калифорний образует три связи с хлором, СО — +3.
- В CfCl2: В лабораторных условиях образуются две связи, СО — +2.
По электронной конфигурации
- Электронная формула калифорния: [Rn] 5f10 7s2.
- Атому калифорния степени окисления +3 достичь проще, так как это дает стабильную полузаполненную или близкую к ней структуру 5f-оболочки.
По химическому соединению (Алгебраический расчет)
Пример для Cf2O3:
Сумма СО равна 0. Кислород -2. Обозначим калифорний как x.
2x + 3 · (-2) = 0 ⇒ 2x = 6 ⇒ x = +3
Примеры степеней окисления калифорния
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Наиболее стабильная. Единственное состояние в растворах. | CfCl3, Cf2O3 |
| +2 | Восстановительная. Получена только в расплавах. | CfCl2 |
| 0 | Металл. Простое вещество, синтезируемое при восстановлении солей. | Cf (металл) |
Шпаргалка для калифорния
- +3 — единственная надежная степень окисления, «родная» для элемента.
- +2 — экспериментальная форма, требующая особых восстановительных условий.
- Радиоактивность — ограничивает химические эксперименты с этим элементом.
Калифорний вне учебника: существуют ли иные состояния?
Высшие степени (+4 и выше): В отличие от урана или плутония, калифорний не проявляет склонности к образованию соединений со степенью окисления выше +3.
Теоретические расчеты показывают, что 5f-электроны калифорния слишком сильно связаны с ядром, чтобы их можно было «оторвать» в обычном химическом процессе.
Отрицательные степени: Для калифорния они невозможны. Атомы с таким большим зарядом ядра и металлической природой не принимают электроны.
Интересный факт: Калифорний — невероятно дорогой материал. Из-за сложности получения (синтезируется в ядерных реакторах) один грамм этого элемента стоит миллионы долларов.
Поэтому вся его химия — это химия микродоз, часто не превышающих нескольких нанограммов.
Пример решения задачи:
▶️ Дано:
Соединение: CfCl3 (трихлорид калифорния).
⌕ Найти:
Определите СО калифорния.
✨ Решение:
Хлор (Cl) имеет заряд -1. В молекуле 3 атома хлора (-3). Чтобы соединение было нейтральным, заряд калифорния должен быть +3.
✅ Ответ:
Cf(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: для калифорния нехарактерны высокие СО, он стабилен только в +3.
Часто задаваемые вопросы
Самая стабильная степень окисления (Cf) — +3.
Это результат достижения энергетически выгодной электронной конфигурации 5f9, которая характерна для середины актиноидного ряда, где удаление электронов с 7s и одного с 5f создает наиболее сбалансированное энергетическое состояние ионов в растворах и твердых соединениях.
В обычных химических условиях — нет. Он гораздо более инертен в этом плане, чем предшествующие ему актиноиды.
По двум фундаментальным причинам:
Электроположительная природа (металл): Для перехода в отрицательную степень окисления атому нужно иметь высокое сродство к электрону, которого у актиноидов нет.
Энергетический барьер 5f-оболочки: Чтобы получить отрицательную степень окисления, атом должен «принять» электрон на свою внешнюю или свободную орбиталь

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.