Теория:
Степень окисления тербия (Tb) в большинстве соединений принимает значение +3, однако для этого элемента также характерна достаточно устойчивая степень +4.
СО +1 теоретически возможна, но крайне редка и мало изучена, а также 0 сам химический элемент.
Тербий является одним из немногих лантаноидов, способных проявлять высокую степень окисления в водных растворах и твердых телах, что связано с особенностями заполнения его f-оболочки.
Например для высшей СО +4: в соединении TbO2 (диоксид тербия) степень окисления металла равна +4.
Это происходит потому, что тербий стремится достичь электронной конфигурации с наполовину заполненным f-подуровнем (4f7), которая обладает повышенной устойчивостью.
Отдавая 4 электрона (два с 6s-подуровня и два с 4f), атом тербия переходит в состояние с симметричной и энергетически выгодной оболочкой.
Для сравнения, наиболее типичная СО +3: встречается в таких соединениях, как TbCl3 (хлорид тербия).
Здесь реализуется стандартный для лантаноидов сценарий: металл отдает три валентных электрона.
Хотя состояние +3 не дает идеально наполовину заполненную f-оболочку (остается 4f8), оно является энергетически сбалансированным и наиболее распространенным для тербия в обычных условиях.
Такие состояния, как +3, доминируют в химии элемента, в то время как форма +4 требует присутствия сильных окислителей, таких как фтор или кислород.
Промежуточные же или иные степени окисления, такие как +1 или +2, для тербия практически не зафиксированы в стабильном виде.
Обладая конфигурацией [Xe] 4f9 6s2, тербию проще всего либо остановиться на классической форме +3, либо дойти до «идеальной» конфигурации f7 в состоянии +4.
Именно поэтому сложные оксиды тербия часто имеют переменный состав (например, Tb4O7), представляя собой смесь состояний +3 и +4.
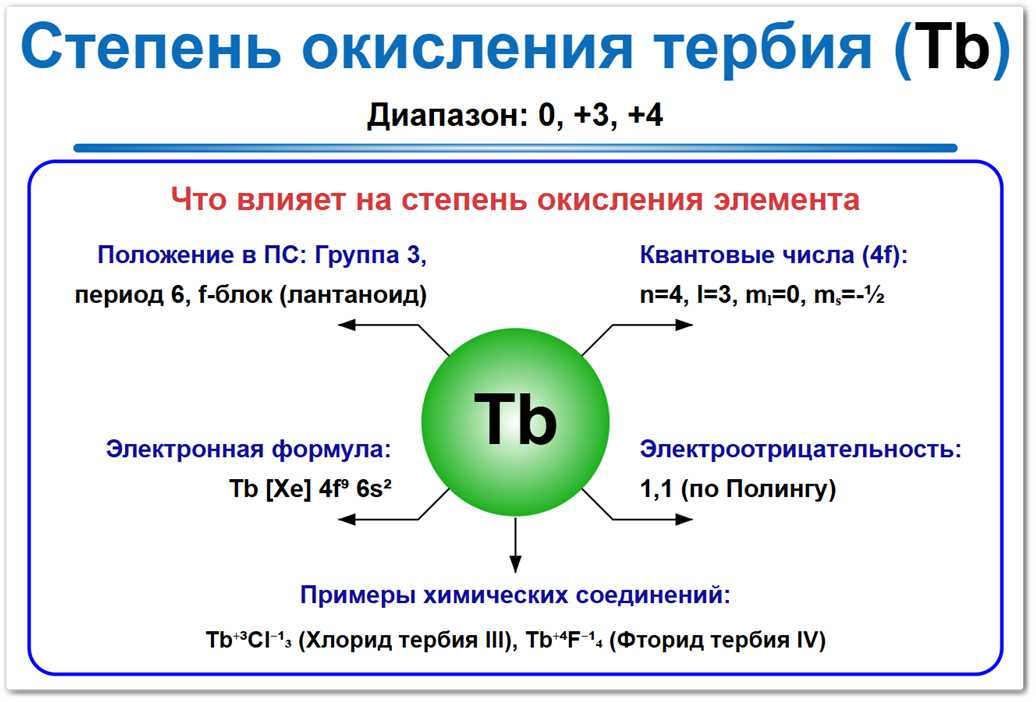
Рис. 1. Возможные степени окисления тербия: основная форма — +3, и уникальная для лантаноидов стабильная высшая форма +4.
Обратите внимание, что химия тербия в плане способности к окислению до +4 схожа с химией церия (Ce) и празеодима (Pr), что позволяет выделять его из смеси других редкоземельных металлов химическими методами.
На формирование его свойств влияют электронное строение (4f9 6s2), эффект «полузаполненной оболочки» и значение электроотрицательности 1,2 по шкале Полинга.
Почему у тербия стабильная степень окисления?
Причина стабильности высшего состояния +4 заключается в стремлении атома оставить на 4f-подуровне ровно 7 электронов, что согласно правилу Хунда соответствует минимальной энергии системы.
- В простом веществе (Tb⁰): Заряд равен 0. Конфигурация:
[Xe] 4f9 6s2. - В ионе (Tb+4): Тербий отдает 4 электрона. Конфигурация:
[Xe] 4f⁷(наполовину заполненный слой).

Рис. 2. Схема перехода тербия в состояние +3: достижение стабильной конфигурации за счет потери двух 6s-электронов и одного 4f-электрона.
Степень окисления тербия в соединениях
В зависимости от условий получения, тербий в соединениях проявляет степень окисления, которая меняет цвет и магнитные свойства вещества:
- Диоксид тербия (TbO2): Tb +4, O -2.
- Оксид тербия(III,IV) (Tb4O7): смесь Tb +3 и +4.
- Тетрафторид тербия (TbF4): Tb +4.
- Хлорид тербия(III) (TbCl3): Tb +3.
- Нитрат тербия(III) (Tb(NO3)3): Tb +3.
Высшая степень окисления
Высшая степень окисления тербия равна +4. Это состояние проявляется в сильных окислах и фторидах, выделяя тербий среди большинства других редкоземельных элементов.
Низшая степень окисления
Хотя в литературе обсуждаются крайне редкие соединения тербия в состоянии +2, общепринято, что степень окисления тербия равна 0 в металлическом виде — это основное низшее состояние.
Промежуточные степени окисления
Степень окисления тербия в веществах часто выглядит как дробная в смешанных оксидах, но на атомном уровне это всегда четкое распределение между формами +3 и +4.
Важно: Именно наличие степени окисления +4 позволяет использовать тербий в создании специальных люминофоров, которые светятся ярко-зеленым цветом при возбуждении.
Почему степень окисления чаще положительная?
Знак заряда обусловлен низкой электроотрицательностью металла и его готовностью отдавать электроны:
- Положительная СО (+): Тербий передает электроны окислителям, обнажая устойчивые внутренние слои.
- Нулевая СО (0): Характерна для чистого металла.
- Отрицательная СО (-): Для тербия не характерна и в обычных условиях не встречается.
Как определить степень окисления тербия
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: варьируются (обычно 3, максимально 4).
- Атомная масса тербия: 159 а.е.м.
По валентности (Число связей)
Как и у других лантаноидов, валентность тербия чаще всего равна III, но может быть и IV.
- В тетрафториде (TbF4): Атом тербия связан с четырьмя атомами фтора. Его валентность — IV, СО — +4.
- В хлориде (TbCl3): Тербий образует три связи с хлором. Валентность — III, СО — +3.
По электронной конфигурации
- Электронная формула тербия: [Xe] 4f9 6s2.
- Атому тербия степени окисления +4 достичь выгодно, так как это дает стабильную конфигурацию 4f7.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Tb4O7 (гептаоксид тетратербия):
Сумма СО равна 0. Кислород -2. Средняя СО тербия x:
4x + 7 · (-2) = 0
4x — 14 = 0 ⇒ x = +3,5 (что означает наличие двух атомов +3 и двух атомов +4).
Примеры степеней окисления тербия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Высшая. Проявляется в жестких условиях окисления. | TbO2, TbF4, BaTbF6 |
| +3 | Наиболее стабильная. Характерна для большинства солей. | TbCl3, Tb2O3, Tb(NO3)3 |
| 0 | Металл. Простое вещество. | Tb (кусок металла) |
Шпаргалка для тербия
- +4 — высшая степень, обусловленная устойчивостью полузаполненного f-слоя.
- Люминесценция — ионы тербия в СО +3 дают чистый зеленый свет (используется в экранах).
- Цвет — соединения Tb(III) обычно бесцветны, а Tb(IV) имеют темную (коричневую) окраску.
Пример решения задачи:
▶️ Дано:
Соединение: TbF4.
⌕ Найти:
Определите СО тербия.
✨ Решение:
Фтор (F) всегда равен -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Tb(+4).
Проверка знаний
Показать ответы
Правильные ответы: 2, 3, 5.
Разбор ошибок:
1 — неверно: тербий является f-элементом (лантаноидом).
4 — неверно: тербий относится к III группе (вместе со всеми лантаноидами), но проявляет СО +4 из-за f-эффекта.
Часто задаваемые вопросы
Самой стабильной СО для него является степень окисления +3.
Да, это одна из его ключевых особенностей. Он проявляет эту степень в оксидах и фторидах.
Нет отрицательной степени окисления по тем же причинам, что и у его соседей по группе лантаноидов:
Низкая электроотрицательность (1.2 по Полингу).
Энергетическая выгода: Тербию гораздо «дешевле» избавиться от 3 или 4 электронов с внешних уровней, чем пытаться удерживать лишние отрицательные заряды.
Стремление к стабильности 4f-слоя.
