Теория:
Степень окисления кюрия (Cm) в химических соединениях представлена ограниченным набором значений, среди которых доминирующим является +3.
Это обусловлено высокой устойчивостью электронной конфигурации с наполовину заполненной f-оболочкой, что делает кюрий типичным представителем ряда актиноидов.
Кроме того, выделяют показатель 0, который относится к кюрию в виде простого вещества (серебристо-белый, интенсивно радиоактивный металл).
Например для наиболее стабильной СО +3: в соединении CmCl3 (хлорид кюрия III) или Cm2O3 (оксид кюрия III) заряд иона равен +3.
В этом состоянии кюрий проявляет выраженное сходство с редкоземельными элементами, такими как гадолиний.
Для сравнения, редкая СО +4: встречается в таких веществах, как CmO2 (диоксид кюрия) или CmF4 (тетрафторид кюрия).
Это состояние менее устойчиво и требует сильных окислителей для своего поддержания.
- Почему +3 так стабильна? Атом кюрия имеет конфигурацию [Rn] 5f7 6d1 7s2. При переходе в состояние +3 он теряет 6d и 7s электроны, оставляя 5f7 — «полузаполненную» оболочку, которая крайне энергетически выгодна.
- Почему +4 сложнее получить? Для достижения СО +4 необходимо затратить значительную энергию на отрыв электрона из стабильной 5f7-оболочки, поэтому такие соединения являются мощными окислителями.
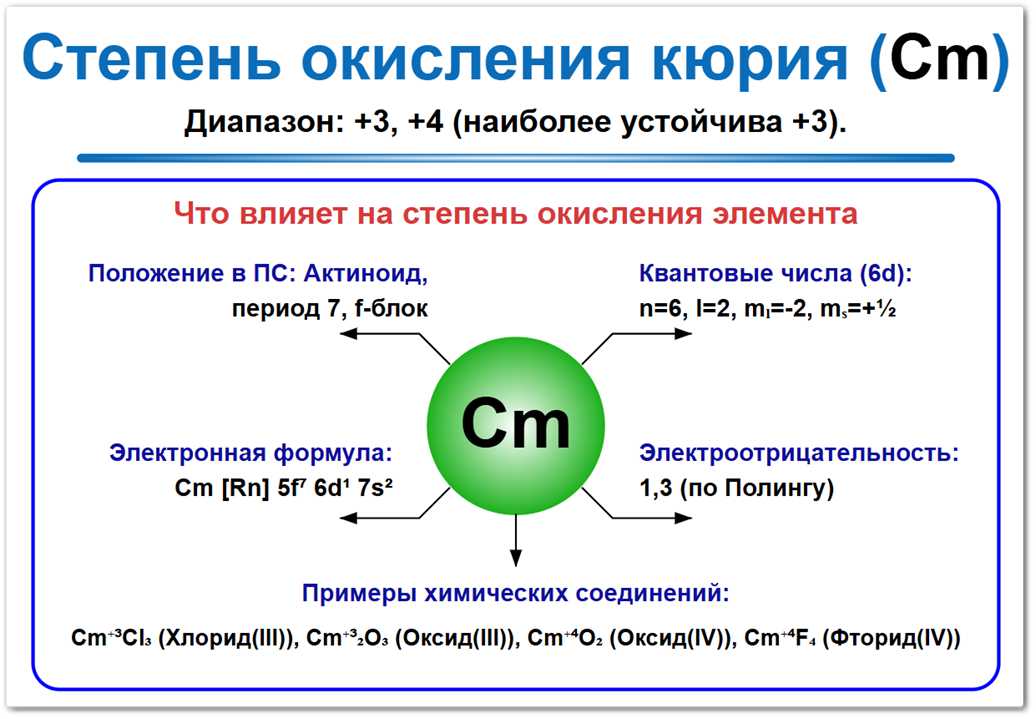
Рис. 1. Основные степени окисления кюрия: 0, +3 и +4.
Состояние +3 является доминирующим в водных растворах, тогда как форма +4 способна существовать лишь в виде твердых соединений или в специальных условиях.
Крайне важно учитывать, что кюрий — это мощный источник альфа-излучения, поэтому его химическое изучение проводится исключительно в специализированных «горячих» камерах с дистанционным управлением.
На химические свойства этого актиноида влияют электронное строение (5f7 6d1 7s2), эффект актиноидного сжатия и значение электроотрицательности 1,28 по Полингу.
Содержание страницы
- 1. Почему +3 — самая устойчивая степень окисления у кюрия
- 2. Степень окисления кюрия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему кюрий предпочитает заряд +3?
- 4. 4 способа определить степень окисления кюрия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления кюрия
- 6. Шпаргалка для кюрия
- 7. Кюрий вне учебника: что скрывает теория?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +3 — самая устойчивая степень окисления у кюрия
Причина стабильности трехвалентного состояния кроется в принципе максимальной устойчивости симметричных электронных подуровней.
- В простом веществе (Cm0): Заряд равен 0. Конфигурация:
[Rn] 5f7 6d1 7s2. - В трехвалентном ионе (Cm+3): Кюрий теряет 2 электрона с 7s и 1 с 6d орбиталей. Конфигурация:
[Rn] 5f7.

Рис. 2. Схема образования степени окисления +3: удаление трех внешних электронов и превращение атома кюрия в стабильный катион Cm3+.
Степень окисления кюрия в соединениях
В зависимости от условий эксперимента, кюрий в соединениях проявляет степень окисления, определяющую его химическое поведение:
- Нитрат кюрия (III) (Cm(NO3)3): Cm +3.
- Оксид кюрия (IV) (CmO2): Cm +4.
- Трихлорид кюрия (CmCl3): Cm +3.
- Оксид кюрия (III) (Cm2O3): Cm +3.
- Фторид кюрия(III) (CmF3): Cm +3.
Высшая степень окисления
Высшая степень окисления Cm равна +4. В этом состоянии он ведет себя как сильный окислитель, стремящийся вернуть электрон для восстановления стабильной конфигурации f7.
Низшая степень окисления
Для кюрия характерна степень окисления 0 в металлическом состоянии. Отрицательные степени для него невозможны из-за его металлической природы.
Промежуточные степени окисления
Степень окисления кюрия в веществах выше +4 (например, +5 или +6) на данный момент не является достоверно доказанной или является крайне сомнительной даже в теории.
Важно: Из-за поразительного сходства ионов Cm3+ и Gd3+ (гадолиния), химики часто используют гадолиний как «неактивный имитатор» кюрия для безопасного исследования свойств его соединений.
Почему кюрий предпочитает заряд +3?
Характер взаимодействия диктуется конфигурацией его 5f-оболочки:
- Положительная СО (+): Кюрий — типичный металл, легко отдающий электроны. СО +3 является «энергетической ямой», в которой атом чувствует себя наиболее комфортно.
- Отсутствие отрицательных СО (-): Как и все актиноиды, кюрий обладает низкой электроотрицательностью и не склонен принимать электроны.
4 способа определить степень окисления кюрия
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 3 электрона, участвующие в образовании связей (6d1 7s2), остальные 5f7 инертны.
- Атомная масса кюрия: 247 а.е.м.
По валентности (Число связей)
Обычно валентность кюрия чаще всего равна III.
- В CmCl3: Кюрий образует три связи с хлором, СО — +3.
- В CmO2: Кюрий образует четыре связи с кислородом, СО — +4.
По электронной конфигурации
- Электронная формула кюрия: [Rn] 5f7 6d1 7s2.
- Атому кюрия степени окисления +3 достичь легче всего, так как это оставляет устойчивый, наполовину заполненный f-слой.
По химическому соединению (Алгебраический расчет)
Пример для CmO2:
Сумма СО равна 0. Кислород -2. Обозначим кюрий как x.
x + 2 · (-2) = 0 ⇒ x — 4 = 0 ⇒ x = +4
Примеры степеней окисления кюрия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Наиболее стабильная. Очень похожа на лантаноиды. | CmCl3, Cm(NO3)3 |
| +4 | Окислительная. Труднодоступна, требует жестких условий. | CmO2, CmF4 |
| 0 | Металл. Простое вещество, сильно радиоактивное. | Cm (металл) |
Шпаргалка для кюрия
- +3 — доминирующая степень, соединения бесцветные или слабо окрашенные.
- +4 — редкое состояние, проявляется в оксидах.
- 5f7-оболочка — секрет стабильности кюрия (III).
Кюрий вне учебника: что скрывает теория?
+2: В отличие от других актиноидов, кюрий (II) до сих пор не был получен даже в самых экстремальных условиях. Энергетическая щель между f7 и f8 слишком велика.
+5 и +6: Несмотря на попытки синтезировать эти состояния (по аналогии с плутонием или америцием), все эксперименты с кюрием потерпели неудачу.
Похоже, +4 — это абсолютный предел для этого элемента.
Отрицательные степени: Невозможны в принципе из-за высокой электроположительности элемента.
Интересный факт: Кюрий саморазогревается! Из-за интенсивного альфа-излучения кусок кюрия может светиться в темноте (из-за ионизации воздуха) и поддерживать температуру выше комнатной без внешнего подогрева. Это делает его уникальным источником тепла в глубоком космосе.
Пример решения задачи:
▶️ Дано:
Соединение: CmF3 (трифторид кюрия).
⌕ Найти:
Определите СО кюрия.
✨ Решение:
Фтор имеет заряд -1. В молекуле 3 атома фтора (суммарно -3). Для нейтральности заряд кюрия равен +3.
✅ Ответ:
Cm(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3.
Разбор ошибок:
2 — неверно: СО +3 является максимально устойчивой для кюрия.
4 — неверно: кюрий — активный металл, он проявляет только положительные СО.
Часто задаваемые вопросы
Это связано с уникальной стабильностью наполовину заполненной f-оболочки (f7). Отрыв электрона из этой оболочки требует колоссальных затрат энергии.
Нет по двум основным причинам:
Высокая электроположительность: Кюрий — это типичный актиноид, чрезвычайно электроположительный металл.
Его атомы стремятся отдать электроны, чтобы достичь стабильной электронной конфигурации, а не принять их для образования отрицательных состояний.
Энергетическая выгода: Для кюрия энергетически выгодно находиться в стабильной степени окисления +3 (полностью заполненная или наполовину заполненная f-оболочка).
Присоединение электронов для создания отрицательного заряда потребовало бы затрат энергии, превышающих выгоду от образования связей, поэтому такие состояния для него нехарактерны.
Самая стабильная +3.
Имеет электронную конфигурацию 5f7 6d1 7s2. При потере трех электронов он образует ион Cm3+ с конфигурацией 5f7.
Эта оболочка заполнена ровно наполовину, что обеспечивает высокую энергетическую стабильность (по правилу Хунда).
Это состояние энергетически наиболее выгодно и трудно поддается изменению.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.