Теория:
Степень окисления кадмия (Cd) практически во всех его соединениях принимает значение +2, что является его наиболее характерным и стабильным состоянием.
Также существуют редкие и крайне неустойчивые состояния с СО +1 (например, в некоторых солях в расплавах), а также состояние 0, характерное для металлической формы.
Например для высшей СО +2: в соединении CdO (оксид кадмия) степень окисления металла равна +2.
Это происходит потому, что кадмий находится в 12-й группе и при взаимодействии с окислителями он отдает два своих внешних электрона с 5s-подуровня (4d10 5s2), достигая устойчивого состояния с полностью заполненным d-слоем.
Для сравнения, редкая СО +1: встречается в таких соединениях, как Cd2[AlCl4]2.
Здесь ситуация необычная: кадмий образует связь Cd–Cd, похожую на ту, что встречается у ртути в ионе [Hg2]2+. В таких структурах формальная степень окисления каждого атома металла равна +1.
Такие состояния крайне нестабильны и при контакте с водой или на воздухе мгновенно диспропорционируют на металлическое серебристое состояние (0) и стабильную форму +2.
Промежуточные же степени окисления, отличные от +2, являются «неудобными» для атома.
Обладая конфигурацией [Kr] 4d10 5s2, кадмию энергетически выгоднее полностью освободить 5s-орбиталь, сохранив симметричную и закрытую 4d10 оболочку.
Именно поэтому химия кадмия гораздо менее разнообразна по степеням окисления, чем химия его соседа по периоду — рутения.
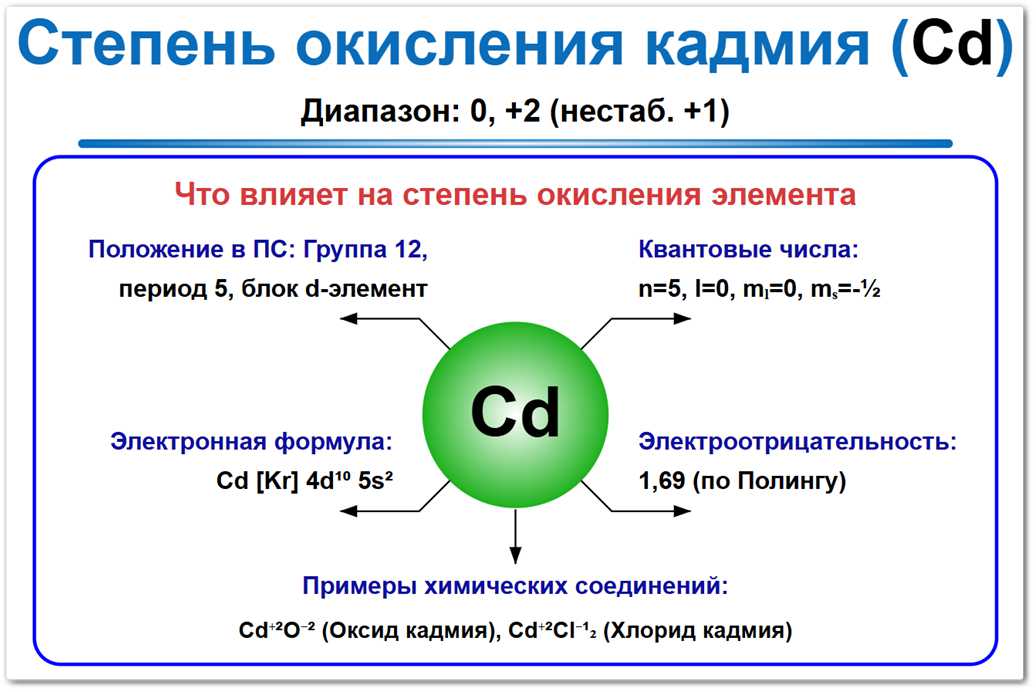
Рис. 1. Возможные степени окисления кадмия: от 0 до +2. Наиболее устойчивая форма — +2 (сульфиды, хлориды), которая встречается почти во всех природных соединениях.
Обратите внимание, что химия кадмия во многом схожа с химией цинка (Zn), своего соседа сверху по группе, что проявляется в исключительной стабильности состояния +2 и отсутствии склонности к образованию высших оксидов.
На формирование свойств влияют электронное строение (4d10 5s2), положение в 12-й группе и значение электроотрицательности 1,7 по шкале Полинга.
Содержание страницы
- 1. Почему у кадмия стабильная степень окисления?
- 2. Степень окисления кадмия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления кадмия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления кадмия
- 6. Шпаргалка для кадмия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у кадмия стабильная степень окисления?
Причина стабильности основного состояния кадмия (+2) заключается в том, что потеря двух 5s-электронов приводит к достижению устойчивой электронной конфигурации с заполненным d-подуровнем.
- В простом веществе (Cd⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 4d [↑↓][↑↓][↑↓][↑↓][↑↓]. - В ионе (Cd+2): Кадмий отдает 2 валентных электрона. Конфигурация:
[Kr] 4d10.
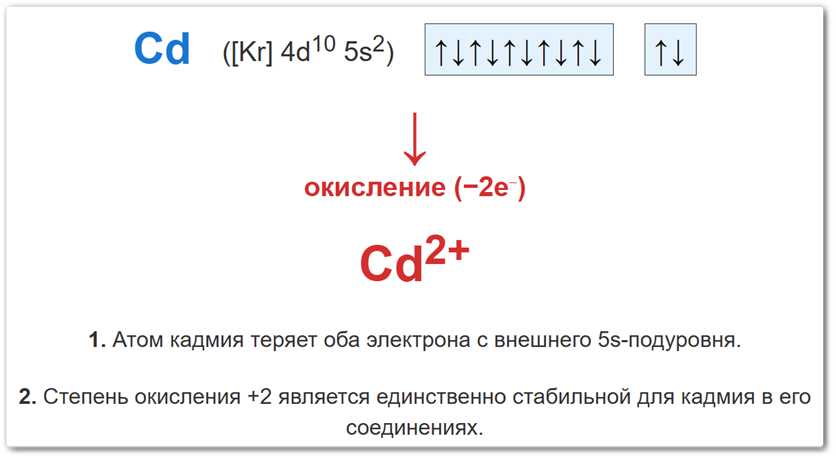
Рис. 2. Процесс окисления кадмия: от металлического состояния до самого стабильного катиона +2.
Степень окисления кадмия в соединениях
В зависимости от аниона, кадмий в соединениях проявляет степень окисления, которая определяет его токсичность и применение в аккумуляторах:
- Сульфид кадмия (CdS): Cd +2, S -2.
- Хлорид кадмия (CdCl2): Cd +2, Cl -1.
- Гидроксид кадмия (Cd(OH)2): Cd +2.
- Тетрахлорокадмат(II) аммония ((NH4)2[CdCl4]): Cd +2.
- Диметилкадмий (Cd(CH3)2): Cd +2.
Высшая степень окисления
Высшая степень окисления кадмия равна +2. В отличие от элементов 8-й или 11-й групп, кадмий крайне неохотно задействует свои d-электроны, поэтому состояния выше +2 для него нехарактерны.
Низшая степень окисления
Для кадмия в металлическом виде степень окисления равна 0 — это типичное состояние для кадмиевых электродов. Отрицательные степени окисления для кадмия не зафиксированы.
Промежуточные степени окисления
Степень окисления кадмия в веществах крайне редко принимает значение +1. Такие соединения существуют только в безводных расплавах и моментально разрушаются в обычных условиях.
Важно: Почти во всех задачах и расчетах степень окисления кадмия формула соединения всегда предполагает заряд +2, что делает его химию предсказуемой и схожей с цинком.
Почему степень окисления чаще положительная?
Знак заряда определяется металлической природой элемента:
- Положительная СО (+): Кадмий отдает электроны неметаллам, достигая стабильной конфигурации d¹⁰.
- Нулевая СО (0): Характерна для чистого металла, используемого для антикоррозийных покрытий.
- Отрицательная СО (-): Физически невозможна из-за низкой электроотрицательности металла.
Как определить степень окисления кадмия
По таблице Менделеева
- Семейство: d-элемент (группа цинка).
- Валентные электроны: 2 (на 5s-подуровне).
- Атомная масса кадмия: 112,4 а.е.м.
По валентности (Число связей)
В отличие от переходных металлов с переменной валентностью, валентность кадмия стабильна и равна II.
- В оксиде кадмия (CdO): Атом кадмия образует две связи с кислородом. Его валентность — II, а степень окисления равна +2.
- В сульфате (CdSO4): Кадмий замещает два атома водорода в кислоте. Валентность — II, СО — +2.
По электронной конфигурации
- Электронная формула кадмия: [Kr] 4d10 5s2.
- Атому кадмия степени окисления +2 достичь выгодно, так как это полностью освобождает внешний 5s-слой.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Cd(NO3)2 (нитрат кадмия):
Сумма СО равна 0. Анион NO₃ имеет заряд -1. Обозначим Cd как x.
x + 2 · (-1) = 0
x — 2 = 0 ⇒ x = +2
Примеры степеней окисления кадмия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +2 | Основная / Высшая. Стабильная форма всех солей. | CdO, CdCl2, CdS, CdSO4 |
| 0 | Металл. Состояние свободного элемента. | Cd (пластина или порошок) |
| +1 | Редчайшая. Существует в виде кластерных ионов. | Cd2Cl2 (в расплавах) |
Шпаргалка для кадмия
- +2 — практически единственная степень окисления в химии.
- Аккумуляторы — никель-кадмиевые батареи основаны на переходе Cd(0) в Cd(+2).
- Цвет — сульфид кадмия (+2) известен как «кадмий желтый», важный пигмент для художников.
Пример решения задачи:
▶️ Дано:
Соединение: CdS (сульфид кадмия).
⌕ Найти:
Определите СО кадмия.
✨ Решение:
Сера (S) в сульфидах проявляет СО -2. Уравнение: x + (-2) = 0 → x = +2.
✅ Ответ:
Cd(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 5.
Разбор ошибок:
2 — неверно: высшая СО кадмия +2, так как он не задействует d-электроны.
4 — неверно: как металл, кадмий не проявляет отрицательных СО.
Часто задаваемые вопросы
Единственной стабильной степенью окисления кадмия является +2.
Кадмий находится в конце d-блока, его 4d-подуровень полностью заполнен и сильно притянут к ядру, поэтому эти электроны не участвуют в окислении.
Металлы (в т. ч. кадмий) в химических соединениях всегда имеют нулевую или положительную степень окисления — отрицательная для них невозможна по природе.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.