Теория:
Степень окисления иттербия в большинстве соединений принимает значение +3, однако для этого элемента также характерно довольно устойчивое состояние +2.
А также 0 сам химический элемент в чистом виде.
В отличие от многих других лантаноидов, иттербий обладает способностью формировать стабильные двухзарядные ионы, что связано с особенностями заполнения его электронной оболочки.
Например для наиболее стабильной СО +3: в соединении Yb2O3 (оксид иттербия III) степень окисления металла равна +3.
Это происходит потому, что иттербий, как и большинство редкоземельных элементов, при химическом взаимодействии отдает три валентных электрона.
При этом его 4f-подуровень остается почти или полностью заполненным, что обеспечивает высокую химическую устойчивость таких соединений.
Для сравнения, СО +2: встречается в таких веществах, как YbCl2 (хлорид иттербия II).
Здесь ситуация иная: иттербий отдает только два электрона с внешнего 6s-уровня, сохраняя полностью заполненную f-оболочку (4f14).
Такая конфигурация обладает повышенной симметрией и энергетической выгодой, что делает состояние +2 для иттербия гораздо более доступным, чем для большинства его соседей по группе лантаноидов.
Такие соединения являются сильными восстановителями, так как металл стремится перейти к более привычному положительному заряду +3, который в водных растворах является доминирующим.
Промежуточные или высшие степени окисления, такие как +4, для иттербия практически невозможны.
Обладая конфигурацией [Xe] 4f14 6s2, атому иттербия энергетически «невыгодно» разрушать полностью завершенный 4f-слой.
Ему проще остановиться на стабильной форме +3, либо сохранить f-оболочку нетронутой в форме +2.
Именно поэтому химия иттербия сосредоточена вокруг этих двух состояний, а резкий переход между ними часто используется в специфических химических синтезах.
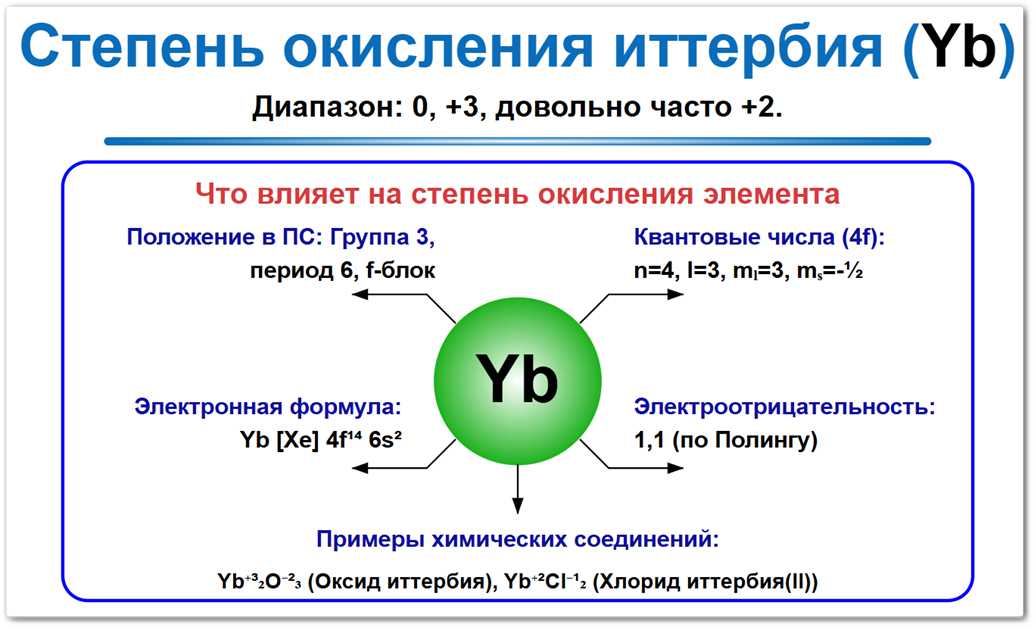
Рис. 1. Возможные степени окисления иттербия: от 0 до +3.
Наиболее устойчивая форма — +3 (оксиды, соли), а уникальная для лантаноидов стабильная форма +2 проявляется в дигалогенидах.
Обратите внимание, что химия иттербия в состоянии +2 имеет сходство с химией щелочноземельных металлов, например кальция (Ca) или стронция (Sr), из-за близости ионных радиусов и схожего характера связей.
На формирование его свойств влияют электронное строение (4f14 6s2), положение в конце ряда лантаноидов и значение электроотрицательности 1,1 по шкале Полинга.
Содержание страницы
- 1. Почему +3 — самая стабильная степень окисления у иттербия
- 2. Степень окисления иттербия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему иттербий почти всегда отдаёт электроны (степени+2, +3), а не принимает?
- 4. 4 способа определить степень окисления иттербия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления иттербия
- 6. Шпаргалка для иттербия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 — самая стабильная степень окисления у иттербия
Причина стабильности состояний иттербия заключается в завершенности 4f-подуровня, что при потере электронов приводит к достижению устойчивой электронной конфигурации.
- В простом веществе (Yb⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 6s2. - В ионе (Yb+2): Иттербий отдает 2 электрона. Конфигурация:
[Xe] 4f14(полностью заполненный слой).

Рис. 2. Процесс окисления иттербия: от металлического состояния до катионов +2 и +3 за счет потери внешних валентных электронов.
Степень окисления иттербия в соединениях
В зависимости от условий реакции, иттербий в соединениях проявляет степень окисления, которая меняет не только химическую активность, но и физические свойства (например, магнитность):
- Оксид иттербия(III) (Yb2O3): Yb +3, O -2.
- Хлорид иттербия(II) (YbCl2): Yb +2, Cl -1.
- Фторид иттербия(III) (YbF3): Yb +3.
- Сульфат иттербия(III) (Yb2(SO4)3): Yb +3.
- Дииодид иттербия (YbI2): Yb +2.
Высшая степень окисления
Высшая степень окисления Yb равна +3. Это значение является пределом для данного элемента в подавляющем большинстве химических систем.
Низшая степень окисления
Для иттербия характерна степень окисления +2, однако атом иттербия имеет степень окисления 0 в металлическом виде — это стандартное состояние для простого вещества.
Промежуточные степени окисления
Степень окисления иттербия в веществах крайне редко отклоняется от значений +2 или +3. В отличие от других металлов, у него нет широкого набора нестабильных промежуточных форм.
Важно: Иттербий в степени окисления +2 обладает уникальными люминесцентными свойствами, что делает его степень окисления иттербия формула соединения (например, в допированных кристаллах) критически важной для лазерной техники.
Почему иттербий почти всегда отдаёт электроны (степени+2, +3), а не принимает?
Знак заряда определяется типичными свойствами лантаноидов и положением элемента в таблице:
- Положительная СО (+): Иттербий легко расстается с внешними электронами, превращаясь в стабильный катион.
- Нулевая СО (0): Характерна для мягкого, серебристого редкоземельного металла.
- Отрицательная СО (-): Для иттербия не зафиксирована, так как его электроотрицательность слишком мала для приема электронов.
4 способа определить степень окисления иттербия
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: 2 (на 6s-подуровне) и потенциально электроны 4f-подуровня.
- Атомная масса иттербия: 173 а.е.м.
По валентности (Число связей)
Как и у большинства лантаноидов, валентность иттербия обычно равна III, но может принимать значение II.
- В оксиде (Yb2O3): Иттербий образует связи, соответствующие валентности III, СО — +3.
- В дииодиде (YbI2): Иттербий проявляет валентность II, СО — +2.
По электронной конфигурации
- Электронная формула иттербия: [Xe] 4f14 6s2.
- Атому иттербия степени окисления +2 достичь легко, так как это оставляет полностью заполненный 4f-подуровень.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для YbCl3 (хлорид иттербия III):
Сумма СО равна 0. Хлор всегда -1. Обозначим Yb как x.
x + 3 · (-1) = 0 ⇒ x = +3
Примеры степеней окисления иттербия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Типичная. Самая стабильная форма для лантаноидов. | Yb2O3, YbCl3, YbF3 |
| +2 | Устойчивая. Характерна для дигалогенидов, сильный восстановитель. | YbCl2, YbI2, YbSO4 |
| 0 | Металл. Состояние чистого химического элемента. | Yb (металл) |
Шпаргалка для иттербия
- +3 — основная степень окисления, наиболее стабильная в растворах.
- +2 — проявляется благодаря полностью заполненному 4f-подуровню (4f14).
- Восстановитель — соединения Yb(+2) легко окисляются до Yb(+3), отдавая электрон.
Пример решения задачи:
▶️ Дано:
Соединение: YbI2 (иодид иттербия II).
⌕ Найти:
Определите СО иттербия.
✨ Решение:
Иод (I) как галоген в данном случае равен -1. Уравнение: x + 2 · (-1) = 0 → x — 2 = 0 → x = +2.
✅ Ответ:
Yb(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: иттербий не является переходным металлом 8-й группы и не может иметь СО +8.
5 — неверно: Yb(+2) стремится отдать электрон и стать Yb(+3), поэтому он является восстановителем, а не окислителем.
Часто задаваемые вопросы
Наиболее стабильной формой в химии является состояние +3.
Да, это один из немногих лантаноидов, для которых СО +2 является химически значимой и устойчивой в определенных соединениях.
Для иттербия достижение СО +4 потребовало бы разрушения завершенной оболочки 4f14, что энергетически невозможно в обычных условиях.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.