Теория:
Степень окисления диспрозия (Dy) в подавляющем большинстве стабильных соединений принимает значение +3, значительно реже встречаются состояния +2 и крайне нестабильное +4.
Как и другие лантаноиды, диспрозий обладает высокой химической активностью.
А его электронное строение позволяет ему легко отдавать внешние электроны для формирования устойчивых химических связей.
Например для наиболее характерной СО +3: в соединении Dy2O3 (оксид диспрозия) степень окисления металла равна +3.
Это происходит потому, что диспрозий относится к f-элементам и при взаимодействии с сильными окислителями он задействует свои валентные электроны (4f10 6s2), достигая стабильного состояния.
Чаще всего отрываются два 6s-электрона и один 4f-электрон, что является энергетически выгодным для этого металла.
Для сравнения, низшая СО +2: встречается в таких галогенидах, как DyI2.
Здесь ситуация иная: металл не полностью отдает электроны со своего валентного слоя.
Такие соединения являются мощными восстановителями и крайне нестабильны в присутствии воды или кислорода.
Так как диспрозий стремится вернуться к положительному заряду +3, который для него энергетически естественнее.
Промежуточные или высшие состояния, такие как +4, встречаются крайне редко (например, в некоторых фторидных комплексах под высоким давлением фтора).
Обладая конфигурацией [Xe] 4f10 6s2, атому диспрозия проще всего расстаться с тремя электронами.
Удаление четвертого электрона требует значительных затрат энергии, так как это нарушает уже относительно стабильную оболочку.
Именно поэтому соединения диспрозия вне степени окисления +3 склонны к быстрому переходу в стандартную форму при малейшем изменении условий среды.
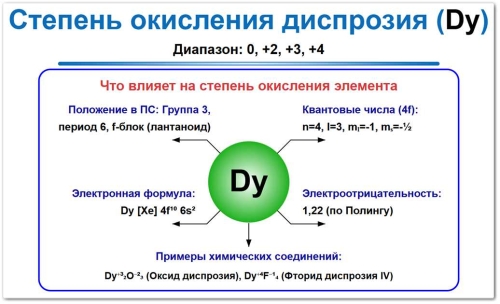
Рис. 1. Возможные степени окисления диспрозия: от 0, +2, +3, +4. Наиболее устойчивая форма — +3 (оксиды, соли), которая является доминирующей в химии этого элемента.
Обратите внимание, что химия диспрозия во многом схожа с химией гольмия (Ho) и тербия (Tb), что проявляется в способности этих металлов образовывать аналогичные по структуре соли и оксиды.
На формирование его свойств влияют электронное строение (4f10 6s2), положение в группе лантаноидов и значение электроотрицательности 1,22 по шкале Полинга.
Почему +3 — самая стабильная степень окисления диспрозия?
Причина стабильности состояния +3 заключается в оптимальном балансе между энергией ионизации и энергией гидратации (или кристаллической решетки), что делает потерю трех электронов наиболее выгодной.
- В простом веществе (Dy⁰): Заряд равен 0. Конфигурация:
[Xe] 4f¹⁰ 6s². - В ионе (Dy+3): Диспрозий отдает 3 валентных электрона. Конфигурация:
[Xe] 4f⁹.
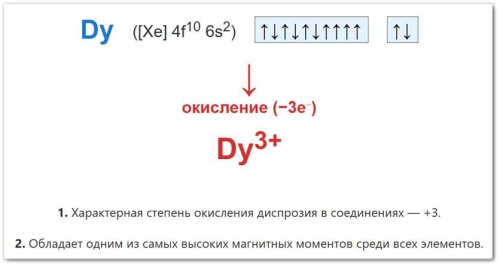
Рис. 2. Процесс превращения атома диспрозия в катион Dy³⁺, обеспечивающий стабильность большинства его химических соединений.
Степень окисления диспрозия в соединениях
В зависимости от реагентов, диспрозий в соединениях проявляет степень окисления, которая определяет магнитные и оптические свойства вещества:
- Оксид диспрозия (Dy2O3): Dy +3, O -2.
- Хлорид диспрозия (DyCl3): Dy +3, Cl -1.
- Дииодид диспрозия (DyI2): Dy +2.
- Фторид диспрозия(III) (DyF3): Dy +3.
- Нитрат диспрозия (Dy(NO3)3): Dy +3.
Высшая степень окисления
Высшая степень окисления Dy равна +4. Однако это состояние является исключительным и достижимо только в присутствии самых агрессивных окислителей, таких как фтор.
Низшая степень окисления
В специфических твердотельных соединениях возможна степень окисления +2.
Однако атом диспрозия имеет степень окисления 0 в металлическом виде — это стандартное состояние для чистого редкоземельного металла.
Промежуточные степени окисления
В большинстве соединений степень окисления диспрозия практически всегда равна +3.
Любые отклонения в сторону +2 или +4 делают вещество крайне реакционноспособным и химически «неудобным» для длительного хранения.
Важно: Состояние +3 — это наиболее химически инертная форма, где степень окисления диспрозия формула соединения (будь то сульфат или фосфат) почти всегда указывает на заряд +3.
Почему диспрозий почти всегда отдаёт электроны (степени +2, +3, +4), а не принимает?
Знак заряда определяется металлической природой элемента и его положением в ряду лантаноидов:
- Положительная СО (+): Диспрозий легко отдает электроны неметаллам, стремясь к устойчивому энергетическому уровню.
- Нулевая СО (0): Характерна для чистого серебристо-серого металла.
- Отрицательная СО (-): Для диспрозия не характерна, так как металлы этой группы не проявляют электроотрицательных свойств.
4 способа определить степень окисления диспрозия
По таблице Менделеева
- Семейство: f-элемент (редкоземельный металл).
- Валентные электроны: 12 (10 на 4f-подуровне и 2 на 6s-подуровне).
- Атомная масса диспрозия: 162,5 а.е.м.
По валентности (Число связей)
В стабильных соединениях валентность диспрозия практически всегда постоянна и равна III.
- В оксиде (Dy2O3): Каждый атом диспрозия образует связи с кислородом, проявляя валентность III, а степень окисления при этом равна +3.
- В хлориде (DyCl3): Диспрозий образует три связи с хлором. Валентность — III, СО — +3.
По электронной конфигурации
- Электронная формула диспрозия: [Xe] 4f10 6s2.
- Атому диспрозия степени окисления +3 достичь выгодно, так как это освобождает внешний 6s-слой и один электрон с f-подуровня.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Dy2(SO4)3 (сульфат диспрозия):
Сумма СО равна 0. Сульфат-ион (SO₄) всегда -2. Обозначим Dy как x.
2 · x + 3 · (-2) = 0
2x — 6 = 0 ⇒ x = +3
Реальные примеры: где встречаются +2, +3 и +4 у диспрозия (оксиды, галогениды, комплексные соединения)
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Высшая. Крайне неустойчива, только в особых условиях. | Cs3[DyF7] |
| +3 | Стабильная. Основная форма для большинства минералов и реактивов. | Dy2O3, DyCl3, DyF3 |
| +2 | Низкая. Сильный восстановитель, встречается в иодидах. | DyI2, DyBr2 |
| 0 | Металл. Чистое вещество с магнитными свойствами. | Dy (металлический) |
Шпаргалка для диспрозия
- +3 — типичная степень, в которой металл проявляет сильные парамагнитные свойства.
- Люминесценция — ионы диспрозия(III) светятся в желтом диапазоне спектра под УФ-лучами.
- Магнетизм — диспрозий имеет один из самых высоких магнитных моментов среди всех элементов.
Пример решения задачи:
▶️ Дано:
Соединение: DyCl3 (хлорид диспрозия).
⌕ Найти:
Определите СО диспрозия.
✨ Решение:
Хлор (Cl) всегда равен -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Dy(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 5.
Разбор ошибок:
3 — неверно: диспрозий — тяжелый редкоземельный металл. Самый легкий — литий.
4 — неверно: СО +2 крайне нестабильна и быстро окисляется до +3.
Часто задаваемые вопросы
Наиболее распространенной и химически устойчивой является степень окисления +3.
Нет, в отличие от рутения, максимальная степень окисления диспрозия ограничена +4, и та встречается крайне редко.
У (Dy) нет отрицательной степени окисления по тем же фундаментальным причинам, что и у других лантаноидов:
1. Низкая электроотрицательность (1.22 по Полингу).
2. Энергетическая выгода: ему гораздо «дешевле» сбросить 3 внешних электрона, чем пытаться удержать лишние отрицательные заряды.
3. Стремление к устойчивости: Затраты энергии на добавление электронов (чтобы стать отрицательным) физически не могут быть скомпенсированы в химических реакциях.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.