Теория:
Степень окисления гольмия (Ho) в подавляющем большинстве стабильных соединений принимает значение +3.
В исключительных случаях и специфических условиях могут встречаться состояния +1, +2, а также 0 сам химический элемент в свободном состоянии.
Как и другие лантаноиды, гольмий проявляет высокую химическую активность, стремясь отдать свои внешние электроны для достижения наиболее устойчивого энергетического состояния.
Например для основной СО +3: в соединении Ho2O3 (оксид гольмия) степень окисления металла равна +3.
Это происходит потому, что гольмий относится к семейству f-элементов и при взаимодействии с кислородом он задействует три валентных электрона (два с 6s-подуровня и один с 4f-подуровня).
Достигая стабильного заряда и устойчивой конфигурации, характерной для редкоземельных металлов.
Для сравнения, редкая СО +2: встречается в некоторых твердотельных галогенидах, например в HoI2.
Здесь ситуация иная: металл не полностью отдает свой валентный потенциал, что делает такие соединения сильными восстановителями.
Подобные состояния крайне нестабильны на воздухе и в водных средах, так как гольмий стремится вернуться к положительному заряду +3, который для него энергетически естественнее.
Высшие же степени окисления, превышающие +3 (например, +4), для гольмия нехарактерны и в обычных химических реакциях не фиксируются.
Обладая электронной конфигурацией [Xe] 4f11 6s2, атому гольмия проще всего расстаться с тремя электронами.
Удаление большего количества электронов потребовало бы разрушения уже достаточно стабильного 4f-подуровня, что энергетически невыгодно.
Именно поэтому химия гольмия считается весьма однообразной в плане валентных состояний — он почти всегда выступает в роли трехзарядного катиона.
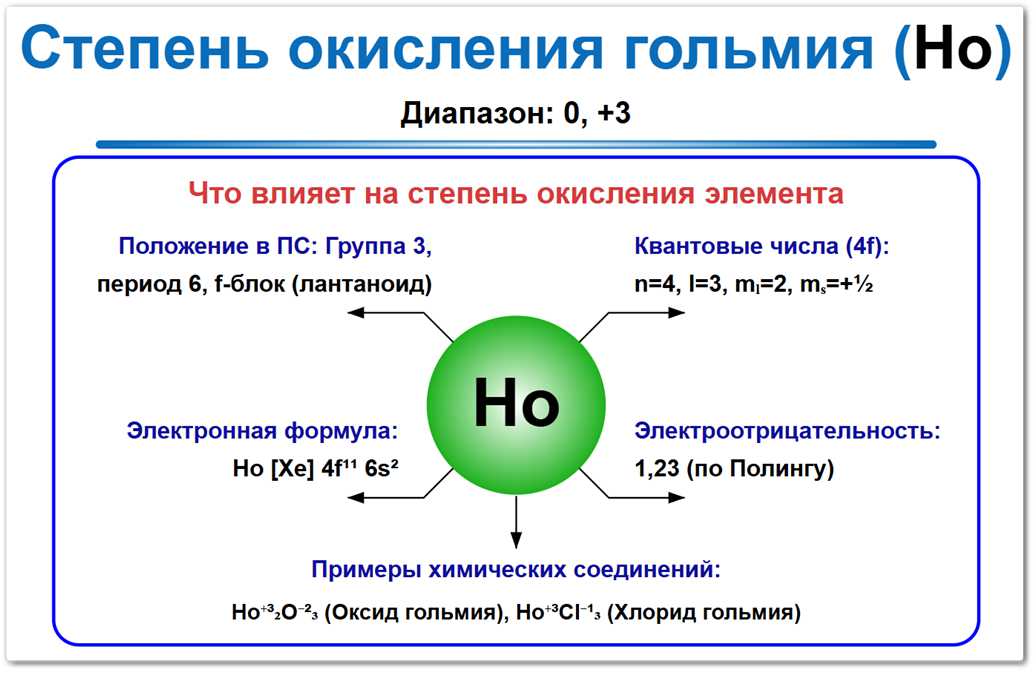
Рис. 1. Возможные степени окисления гольмия: наиболее устойчивая форма — +3.
Состояния ниже +3 характерны только для некоторых кластерных соединений и металлоорганических комплексов.
Обратите внимание, что химия гольмия во многом схожа с химией диспрозия (Dy) и эрбия (Er), его соседей по ряду лантаноидов, что обусловлено близкими радиусами ионов и схожим строением электронных оболочек.
На их формирование влияют электронное строение (4f11 6s2), эффект «лантаноидного сжатия» и значение электроотрицательности 1,23 по шкале Полинга.
Содержание страницы
- 1. Почему +3 — самая стабильная степень окисления у гольмия?
- 2. Степень окисления гольмия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему гольмий почти всегда отдаёт электроны (степени +1, +2, +3), а не принимает?
- 4. 4 способа определить степень окисления гольмия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Реальные примеры: где встречаются +1, +2, +3 у гольмия (оксиды, галогениды)
- 6. Шпаргалка для гольмия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 — самая стабильная степень окисления у гольмия?
Причина стабильности состояния +3 заключается в оптимальном балансе между энергией ионизации и энергией кристаллической решетки образующихся соединений.
- В простом веществе (Ho0): Заряд равен 0. Конфигурация:
[Xe] 4f11 6s2. - В ионе (Ho+3): Гольмий отдает 3 валентных электрона. Конфигурация:
[Xe] 4f10.

Рис. 2. Процесс превращения металлического гольмия в катион Ho3+, являющийся основой его химических свойств.
Степень окисления гольмия в соединениях
В зависимости от реагентов, гольмий в соединениях проявляет степень окисления, которая определяет цвет и магнитные свойства вещества:
- Оксид гольмия (Ho2O3): Ho +3, O -2.
- Хлорид гольмия (HoCl3): Ho +3, Cl -1.
- Нитрат гольмия (Ho(NO3)3): Ho +3.
- Фторид гольмия (HoF3): Ho +3.
- Дииодид гольмия (HoI2): Ho +2.
Высшая степень окисления
Высшая степень окисления Ho равна +3. В отличие от некоторых других лантаноидов (церия или празеодима), гольмий не способен достигать состояния +4 в стабильных химических соединениях.
Низшая степень окисления
Для гольмия в исключительных случаях возможна степень окисления +2, однако атом диспрозия имеет степень окисления 0 в металлическом виде — это наиболее типичное состояние для простого вещества.
Промежуточные степени окисления
Степень окисления гольмия в веществах крайне редко принимает значения отличные от +3.
Формально выделяемые низшие состояния обычно склонны к быстрому окислению до устойчивого трехзарядного иона.
Важно: Именно состояние +3 с конфигурацией 4f10 обеспечивает гольмию один из самых высоких магнитных моментов среди всех элементов, что делает его незаменимым в производстве сверхмощных магнитов.
Почему гольмий почти всегда отдаёт электроны (степени +1, +2, +3), а не принимает?
Знак заряда определяется металлической природой элемента и его низкой способностью удерживать внешние электроны:
- Положительная СО (+): Гольмий отдает электроны активным неметаллам, образуя ионные связи.
- Нулевая СО (0): Характерна для чистого редкоземельного металла.
- Отрицательная СО (-): Для гольмия физически невозможна, так как он обладает выраженными металлическими свойствами.
4 способа определить степень окисления гольмия
По таблице Менделеева
- Семейство: f-элемент (лантаноид).
- Валентные электроны: 3 электрона (два на 6s и один на 4f подуровнях участвуют в реакциях чаще всего).
- Атомная масса гольмия: 164,9 а.е.м.
По валентности (Число связей)
В подавляющем большинстве случаев валентность гольмия постоянна и равна III.
- В оксиде (Ho2O3): Атом гольмия образует три связи с кислородом. Его валентность — III, а степень окисления равна +3.
- В хлориде (HoCl3): Гольмий связан с тремя атомами хлора. Валентность — III, СО гольмия — +3.
По электронной конфигурации
- Электронная формула гольмия: [Xe] 4f11 6s2.
- Атому гольмия степени окисления +3 достичь выгодно, так как это приводит к удалению внешнего 6s-слоя и частичному освобождению f-орбиталей.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для HoPO4 (фосфат гольмия):
Сумма СО равна 0. Фосфат-ион (PO₄) в сумме имеет заряд -3. Обозначим Ho как x.
x + (-3) = 0 ⇒ x = +3
Реальные примеры: где встречаются +1, +2, +3 у гольмия (оксиды, галогениды)
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Наиболее стабильная. Основная химия элемента. | Ho2O3, HoCl3, HoF3 |
| +2 | Низкая. Встречается в редких дигалогенидах. | HoI2 |
| 0 | Металл. Состояние простого вещества. | Ho (слиток) |
Шпаргалка для гольмия
- +3 — единственная практически важная степень окисления.
- Окраска — ионы гольмия +3 придают кристаллам и стеклам красивый желтый или розоватый оттенок.
- Магнетизм — в СО +3 гольмий обладает исключительными магнитными свойствами.
Пример решения задачи:
▶️ Дано:
Соединение: Ho(OH)3 (гидроксид гольмия).
⌕ Найти:
Определите СО гольмия.
✨ Решение:
Группа OH всегда имеет заряд -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Ho(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4, 5.
Разбор ошибок:
2 — неверно: гольмий не способен достигать таких высоких степеней окисления; его предел — +3.
Часто задаваемые вопросы
Для него стабильной и практически единственной в химии является степень окисления +3.
Нет, как типичный металл он проявляет только положительные или нулевое значения.
Это связано с особенностями строения f-оболочки лантаноидов, которая сильно экранирована, что делает участие большего числа электронов в связях энергетически невозможным.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.