Теория:
Степень окисления германия (Ge) в наиболее устойчивых соединениях равна +4. Это состояние является типичным для элементов его группы.
Значения 0, +2 и -4 встречаются реже. Состояние +2 характерно для некоторых стабильных галогенидов (например, GeCl2) и оксида GeO, однако они проявляют сильные восстановительные свойства, стремясь перейти в +4.
Германий находится в 14-й группе (главная подгруппа IV группы) и является p-элементом 4-го периода.
Как p-элемент, он обладает электронной конфигурацией [Ar] 3d104s24p2. В отличие от галлия, у германия на внешнем p-слое находится уже два электрона.
Германий проявляет преимущественную степень окисления +4. Это связано с тем, что атом может задействовать в образовании связей все четыре внешних электрона (два 4s и два 4p). Полностью заполненный уровень 3d10 остается инертным.
В отличие от кремния, германий чаще проявляет состояние +2 за счет «эффекта инертной пары» s-электронов, что сближает его свойства с оловом.
Чтобы определить возможные значения, используют электронную формулу.
Например:
- Для германия (1s22s22p63s23p63d104s24p2) — потеря всех четырех внешних электронов (s и p) дает устойчивую СО +4.
- Для галлия (1s22s22p63s23p63d104s24p1) — наличие только одного p-электрона ограничивает максимальную СО значением +3.
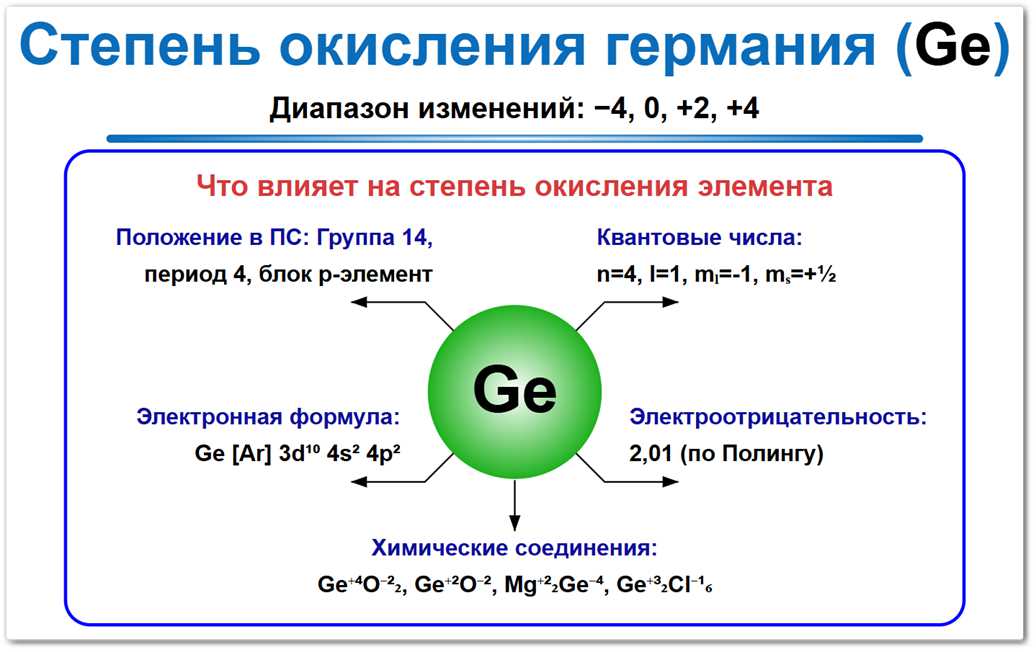
Рис. 1. Возможные степени окисления германия: -4, 0, +2, +4. Обратите внимание, что он может также проявлять степень окисления +1, +3.
На их формирование влияют электронное строение (наличие двух p-электронов), положение в 14-й группе и значение электроотрицательности 2,01 по шкале Полинга.
Содержание страницы
- 1. Почему у германия переменные степени окисления?
- 2. Степень окисления германия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. Почему степень окисления может быть положительной или отрицательной?
- 4. Как определить степень окисления германия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления германия
- 6. Шпаргалка для германия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у германия переменные степени окисления?
Причина гибкости германия — возможность как частичного отрыва p-электронов (СО +2), так и полного вовлечения всей внешней оболочки (СО +4) в химическую связь.
- В простом веществе (Ge⁰): Заряд равен 0. Конфигурация:
4s [↑↓] 4p [↑][↑][ ]. - В ионе (Ge+2): Германий отдает 2 электрона с 4p-уровня. Конфигурация
4s [↑↓] 4p [ ][ ][ ]. - В ионе (Ge+4): Германий отдает 2 электрона с 4p и 2 электрона с 4s. Конфигурация
4s [ ] 4p [ ][ ][ ].

Рис. 2. Процесс окисления германия: атом Ge ([Ar] 3d10 4s2 4p2) теряет внешние электроны, образуя стабильный катион германия (IV).
Степень окисления германия в соединениях
Соединения германия демонстрируют его амфотерную природу с преобладанием кислотных свойств в высшей СО:
- Диоксид германия (GeO2): Ge +4, O -2 (белый порошок).
- Хлорид германия(IV) (GeCl4): Ge +4, Cl -1.
- Германат натрия (Na2GeO3): Ge +4.
- Сульфид германия(II) (GeS): Ge +2, S -2.
- Герман (GeH4): Ge -4, H +1.
Высшая степень окисления
Высшая степень окисления германия равна +4. Она соответствует номеру его группы (IVА) в таблице Менделеева.
Низшая степень окисления
Низшая равна -4. Она проявляется в соединениях с водородом (германах) и активными металлами (германидах).
Важно: В отличие от углерода, для германия отрицательная степень окисления -4 встречается гораздо реже из-за его более металлических свойств.
Почему степень окисления может быть положительной или отрицательной?
Знак заряда зависит от разности электроотрицательности (ЭО).
- Положительная СО (+): Германий отдает электроны более сильным неметаллам (O, Cl, F).
- Отрицательная СО (-): Проявляется в соединениях с водородом (GeH₄) или металлами (Mg₂Ge), где германий сильнее притягивает электронную плотность.
- Нулевая СО (0): Характерна для чистого кристаллического германия (полупроводник).
Как определить степень окисления германия
По таблице Менделеева
- Семейство: p-элемент (группа углерода).
- Валентные электроны: 4 (2 на s-уровне и 2 на p-уровне).
- Атомная масса германия: 72,63 а.е.м. Для сравнения масс других элементов используй таблицу атомных масс.
- Типичная СО: +4.
По валентности (Число связей)
Валентность германия равна II или IV.
- Валентность IV: Соответствует высшей СО +4.
- Пример: GeO2. Здесь германий четырехвалентен.
По электронной конфигурации
- Электронная формула германия: [Ar] 3d10 4s2 4p2. Для просмотра значений (n, l, ml, ms) каждого электрона используй таблицу квантовых чисел.
- Наличие двух p-электронов и двух s-электронов объясняет устойчивость СО +4 и возможность существования СО +2.
По химическому соединению (Алгебраический расчет)
Так как Германий — полуметалл 14-й группы, его высшая степень окисления в сложных веществах практически всегда +4.
Это правило помогает находить степени окисления других элементов в молекуле через простое уравнение.
Пример для GeCl4 (хлорид германия IV):
Сумма всех степеней окисления в молекуле равна 0.
Обозначим СО германия за x, а у хлора (как у типичного галогена в солях) она равна -1.
1 · x + 4 · (-1) = 0
x — 4 = 0 ⇒ x = +4
Примеры степеней окисления германия
| СО | Цвет соединений | Примеры соединений (с индексами) |
|---|---|---|
| +4 | Белый / Бесцветный | GeO2, GeCl4, GeS2 |
| +2 | Черный / Желтый | GeO, GeCl2, GeS |
| 0 | Серый металлик | Ge (Германий) |
| -4 | Газообразное состояние | GeH4, Mg2Ge |
Шпаргалка для германия
- 0 — чистый кристалл (полупроводник, основа электроники).
- +4 — высшая и самая устойчивая форма.
- Амфотерность — GeO₂ проявляет как кислотные, так и слабые основные свойства.
- -4 — проявляется в летучем водородном соединении германе (GeH4).
Пример решения задачи:
▶️ Дано:
Соединение: GeCl4.
⌕ Найти:
Определите СО германия.
✨ Решение:
Хлор (Cl) имеет СО −1. Следовательно: x + 4 · (−1) = 0 → x = +4.
✅ Ответ:
Ge(+4).
Проверка знаний
Отметьте правильные утверждения для Германия (Ge):
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: германий — это полуметалл.
5 — неверно: в GeH4 у германия отрицательная СО (-4).
Часто задаваемые вопросы
Наиболее устойчивой является степень окисления +4. Большинство природных соединений и технических материалов на основе германия содержат его именно в этом состоянии.
В GeO германий имеет СО +2 (неустойчив, восстановитель), а в GeO2 — СО +4 (стабильный диоксид, основа германатных стекол).

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.