Карбонат цинка это белый кристаллический порошок также известный как смитсонит или каламин или цинковый шпат.
Он был назван в честь ученого (английский) Джеймса Смитсона. Это руда цинка, формула карбоната цинка ZnCO3.
Ранее смитсонит путали с гемиморфитом, прежде чем поняли, что оба они были двумя разными минералами.
Оба минерала имеют схожий внешний вид, и термин каламин используется для обоих из них, что привело к этой путанице.

Содержание страницы
Что такое карбонат цинка
Это белое и непахучее кристаллическое твердое тело, субмикрон, или нано-порошок и неразрешим в воде, спирте, или ацетоне но слабо растворим в аммиаке.
Растворим в щелочах и кислотах. Карбонат цинка является важным источником цинка, потому что он может быть легко преобразован в другие соединения цинка, такие как оксид цинка.
Процесс может быть достигнут путем нагревания, что приводит к образованию оксида цинка и углекислого газа. Этот процесс также известен как кальцинирование.
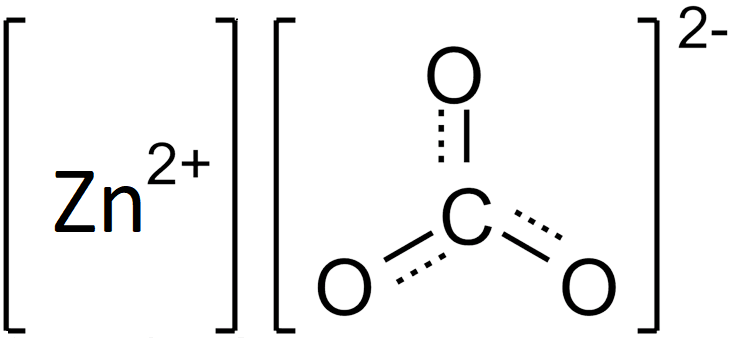
Структура карбоната цинка
Ниже приведена структура карбоната цинка:
Физические свойства карбоната цинка
-
Молекулярная масса карбоната цинка составляет 125,38 г/моль.
-
Температура кипения карбоната цинка составляет 333,6 °C.
-
Температура плавления карбоната цинка составляет 1970 °C.
-
Плотность карбоната цинка составляет 3,5 г/см3.
-
Это белый порошок и имеет слабый запах уксуса.
-
Он является основным по своей природе, поэтому уровень рН выше 10.
-
Нерастворим в воде.
Химические свойства карбоната цинка
Карбонат цинка реагирует с кислотами с образованием хлорида цинка и выделяет углекислый газ.
ZnCO3 + HCl → ZnCl2 + CO2
ZnCO3 + H2SO4 → ZnSO4 + CO2 + H2O
Карбонат цинка при реакции разложения образует оксид цинка и выделяет углекислый газ.
ZnCO3 → ZnO + CO2
Гидротермальный синтез карбоната цинка является результатом реакции между ZnCl2 и K2CO3.
ZnCl2 (aq) + K2CO3 (aq) → ZnCO3 (s) + 2KCl (aq)
Применение карбоната цинка
-
Это неорганическая соль и обычно используется в качестве катализатора в реакциях органического синтеза.
-
Это подходящий прекурсор для изготовления частиц оксида цинка.
-
Он широко используется в производстве резины в качестве сырья. Он добавляется для улучшения прозрачности или прозрачности натурального каучука, поскольку эти два материала имеют очень сравнительный показатель преломления.
-
Благодаря своим фунгицидным и антисептическим свойствам. Он используется в широком спектре продуктов, таких как ванна, макияж, личная чистота, бритье, уход за полостью рта, а также средства по уходу за кожей и волосами.
-
Он также используется в кормовых добавках для животных. Недостаток карбоната цинка может ограничить рост животного, потому что он вносит важный вклад в развитие кости.
-
карбонат цинка также используется в нефтяной промышленности в качестве поглотителя серы.
-
Применяется при напылении воспаленных поверхностей в качестве вяжущего и абсорбирующего средства.
-
Благодаря своим антисептическим свойствам он часто используется в фармацевтике.
Где будет применяться карбонат цинка
Карбонат цинка является рудой цинка и является важным материалом во многих областях применения. Спрос на карбонат цинка растет, потому что его области применения, такие как косметика, сельское хозяйство или производство резины, растут быстрыми темпами.
В зависимости от его применения, масштаба производства или структуры существуют различные пути синтеза карбоната цинка. Нанопорошок цинка может широко использоваться в таких областях, как производство резины, дыхательные системы или косметика.
Размер порошка значительно влияет на производительность материала. Наконец, использование карбоната цинка, по-видимому, увеличится в будущем из-за растущей косметической, резиновой и сельскохозяйственной промышленности.
Часто задаваемые вопросы ответы об карбонате цинка?
Является ли карбонат цинка токсичным?
Да, он токсичен по своей природе, ниже приведены некоторые эффекты карбоната цинка:
- Карбонат цинка может влиять при непосредственном вдыхании.
- Прямой контакт может раздражать кожу и глаза.
- Прямое дыхание может вызвать кашель и свистящее дыхание.
- Высокое воздействие может повредить печень.
Что происходит при прокаливании карбоната цинка?
Когда карбонат цинка нагревается в процессе прокаливания, он превращается в оксид цинка, а затем легко превращается в металл.
При нагревании карбонат цинка находится в белой порошкообразной твердой форме, дает углекислый газ и желтое твердое вещество оксида цинка. Поскольку он образует другой продукт, он будет подвергаться химическим изменениям.
При охлаждении желтое твердое вещество превращается в белый цвет, что является физическим изменением.
Процесс включает в себя как физические, так и химические изменения. Нагрев карбоната цинка-это химическое изменение, а затем охлаждение полученного продукта-физическое изменение.
ZnCO3 → ZnO + CO2
Каковы соответствующие дозы цинка?
Риск заболевания почек увеличивается при низком содержании цинка в рационе. Люди с гемодиализным заболеванием почек также подвержены риску дефицита цинка и нуждаются в добавке цинка для правильного функционирования.
Вегетарианские диеты часто связаны с более низким уровнем поглощения цинка. Эта форма диеты также является одним из факторов риска истощения цинка.
Но в долгосрочной перспективе организм может адаптироваться. Поглощение цинка и исключение потери цинка получат более сильным.
Чрезмерное длительное употребление алкоголя также связано с низким усвоением цинка в организме.
