Восстановление цианистых растворов
Лучший вариант (наиболее полное оборачивание) ограничен «утомляемостью» растворов, которые по мере накопления в них цианистых комплексов меди, цинка, железа и других соединений
все хуже выщелачивают золото, несмотря на подкрепление их свежим цианидом. Утомляемость становится заметной уже в присутствии 0,03% меди или 0,05% цинка.
Ослабление активности растворов объясняют образованием на золоте адсорбционных или иных пленок, существование которых подтверждено, радиохимически М. Д. Ивановским. Вместе с тем, надо обратить внимание и на постепенное повышение ионной силы, особенно быстрое при многозарядных ионах. Указанные выше концентрации соответствуют 4,6•10-3 моль/л Na3Cu (CN)4 и 7,6•10-3 моль/л Na2Zn (CN)4.
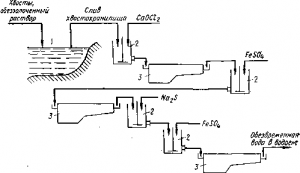
Рис. Схема очистки сточных растворов золотоизвлекательных фабрик: 1 — хвостохранилище; 2 — мешалки; 3 — отстойники
Из выражения для ионной силы:
μ = 1:2(AZ2A + BZ2B + …)
где Л, В, … — концентрации ионов, a Z — их заряды, получим
μCu= (3•4,6•10-3 + 4,6•10-3 •32):2 = 2,8•10-2 г-ион•л,
μZn = (2•7,6•10-3 + 7,6•10-3 •22):2 = 2,3•10-2 г-ион/л,
суммарно μ ≈ 5•10-2.
Снижение активности цианида, казалось бы, невелико, однако оно может быть существенным, если учесть высокий показатель степени, в которой aCN- входит в уравнение.
Основную массу раствора после осаждения золота возвращают на выщелачивание; однако часть его в виде бедных промывных растворов приходится сбрасывать в отвал, иначе не удавалось бы компенсировать постоянный приход воды на промывку хвостов и осадков. Сточные воды несут с собой небольшие количества цианистого натрия, а также ионы Fe(CN)46—,
Cu(CN)n(n-1)-, Zn(CN)24—, SCN—, CNO— и другие соединения.
На рис. приведен один из многих способов обезвреживания. В хранилище для отходов, представляющее собой искусственный прудок, поступают хвосты цианирования и обеззолоченные растворы. Из верхнего осветленного слоя жидкость периодичеоси набирают в мешалку, где ее обрабатывают хлорной известью. Цианид и содержащие его комплексные соединения окисляются до цианата, который в свою очередь гидролизуется:
CN— + ОСl— = CNC— + Сl—CNO- + 2Н2O = NH+4 + СО23—
Цианирование с применением ионообменных смол.
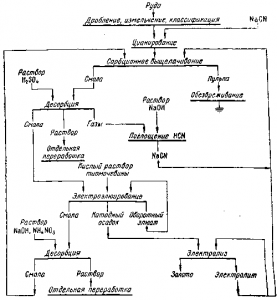
Рис. 2 . Пример схемы сорбционного выщелачивания золота
Многие недостатки цианистого процесса: малая интенсивность, многостадийность, необходимость больших масс токсичных растворов и громоздкого крупногабаритного оборудования, постоянно привлекают внимание исследователей, стремящихся выбрать иные реагенты для выщелачивания, либо изменить переработку растворов. Одним из удачных решений в этой области оказалось разработанное под руководством И. Н. Плаксина и Б. Н. Ласкорина сорбционное выщелачивание, теперь уже успешно применяемое на некоторых крупных золотоизвлекательных фабриках.
В этой технологии для выщелачивания оставлены прежние реагенты — цианид и кислород воздуха; однако в пульпу вводят еще и ионообменную смолу — анионит, которая одновременно с выщелачиванием сорбирует растворенное золото.
Ионообменные смолы — катиониты и аниониты — твердые органические полимеры. Химические структуры их характерны пространственными сетками из углеводородных цепей, несущими ионообменные группы. У катионитов это, например, —СООН или HSO3, способные обменивать водород на катионы. У анионитов аминогруппы различного замещения присоединяют гидроксил либо иной анион. Четырехзамещенный аммоний, связанный с анионами подобно катионам сильных электролитов, дает сильноосновные аниониты, способные к ионообмену в кислой и основной средах. Некоторые иониты бифункциональны — содержат разные ионообменные группы.
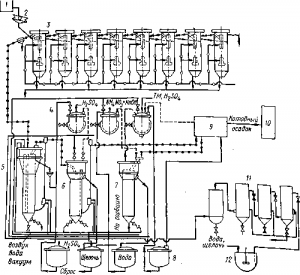
Рис. 3. Цепь аппаратов для работы по схеме рис. 2:
1 — пульпа; 2 — грохот; 3— пачуки для сорбционного выщелачивания; 4 — чаны для растворов десорбентов; 5—колонна для отмывки смолы от частиц руды; 6, 7 — колонна для десорбции примесей; 8 — сборник растворов электроэлюирования; 9, 10—. установки для электроэлюирования и переосаждения золота электролизом; 11 — поглотители цианистого водорода; 12 — сборник щелочных растворов цианида натрия
Обозначив сложную структуру смолы буквой R и отметив твердофазность ее верхней черточкой, запишем:
(R ≡ N)2SO4 + Au(CN)2— = 2R ≡ NAu (CN)2 + SO24—
Подобно Au(CN)2— сорбируются и другие анионы — Fe(CN)4-, Cu(CN)3-, ОН- Zn(CN)f- . В нагруженной смоле,-обменная емкость которой (СОЕ) от 3 до 10 мг/экв/г, после сорбции из цианистого раствора обнаруживаются, например, следующие количества металлов:
| Металл | Au
1,5—8 |
Ag Zn
3 2 |
Fe Cu
3 5 |
| Концентрация,
мг/г |
Одна из возможностей отделения примесей связана с избирательной сорбцией, другая — с десорбцией. При этом используется как различие устойчивости комплексных ионов, так и прочность связи их со смолой. Схема рис. 2, которую надо считать примерной, а отнюдь не оптимальной, показывает последовательность десорбции примесей, а затем и благородных металлов разными реагентами. Последним вытесняется золото, которое одновременно переводится из цианистого в тиомочевинный комплекс:
2R ≡ NAu (CN)2 + 2SC(NH2)2 + SO24— + 4Н+ = (R ≡* N)2SО4 + Au (SCN2H4)2 + 4HCN
(* значение 4)
Из кислых растворов тиомочевины золото осаждают электролизом, который иногда совмещают с элюированием, заставляя нагруженную смолу непрерывно проходить через электролитную ванну особого устройства — электроэлюирование. Чтобы избежать анодного окисления тиомочевины, графитовые аноды отделяют от титановых катодов анионитовыми или катионооб-менными мембранами — тонкими пленками из соответствующих смол. Первые непроницаемы для катионов и нейтральных молекул SC(NН2)2, а вторые задерживают анионы и нейтральные молекулы.
Для пояснения рис. 2 надо сказать, что после обычного выщелачивания части золота в мешалках, протекающего медленнее сорбции, пульпу подают в цепь пачуков особого устройства (рис. 3), где металл доизвлекается из руды и одновременно поглощается смолой. Зерна ионита крупностью 0,4—1,6 мм больше частиц руды, измельченной до минус 0,1 мм, они отделяются на металлических или пластмассовых сетках, установленных в каждом чане. Смола передается в предыдущий, а пульпа — в последующий пачук, как показано на схеме рис. 4.
Нагруженную смолу обмывают для удаления захваченной пульпы и обрабатывают для десорбции примесей цинка и никеля раствором серной кислоты.
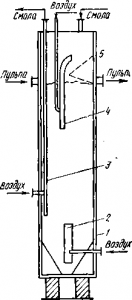
Рис. 4. Пачук для сорбционного выщелачивания:
1 — чан; 2 — аэролифт для перемешивания; 8 — аэролифт для передачи смолы в цепь; 4 — то же, для подачи пульпы на разделительную сетку
Me(CN)n(n-2)- + n Н+ = Ме2+ + n HCN
Электроэлюированием в течение 6—8 ч осаждают на катодах до 90% золота и серебра. Примесь меди, наиболее прочно связанная со смолой, частично остается. Потом ее доизвлекают вместе с железом и кобальтом, действуя щелочным раствором нитрата аммония, и возвращают ионит на сорбционное выщелачивание.
Статья на тему Оборачивание цианистых растворов, Восстановление цианистых растворов

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.