Свойства меди это сходство по свойствам с предшествующими ей переходными металлами третьего периода — кобальтом, никелем и последующим цинком.
Однако и отличается от них присутствием на внешней оболочке атома одного s-электрона, а на предыдущей десяти d-электронов. Эта особенность объясняет наличие трех степеней окисления.

Содержание страницы
Что такое свойства меди и солей
Соединения Cu (III)—сильные окислители, образование их возможно только в особых условиях, Cu (II) устойчива при низких, a Cu (I) при сравнительно высоких температурах.
Из диаграммы состояния системы Сu—О (рис.) видна стабильность Cu2O выше 375° С.
Металл окисляется на воздухе, не содержащем паров воды и СО2, до СuО, а в присутствии этих веществ образуется зеленая поверхностная пленка основных карбонатов Cu (II).
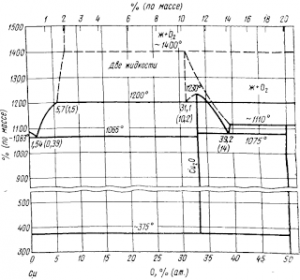
Рис. Диаграмма состояния системы Сu—О.
На воздухе СuО устойчива до 800° С, а в кислороде до 1100° С.
Закись меди Сu2О
Закись Сu2О растворима в жидкой меди, содержание кислорода в металле при 1200° С достигает 1,5%. Дальнейшее нагревание в окислительной среде приводит к образованию расслаивающихся насыщенных растворов (см. рис.).
Растворимость кислорода в твердой меди очень мала и не превышает 0,01%, он присутствует в металле преимущественно в виде отдельной фазы Cu2O.
Из термодинамических данных следует, что Cu2О и СuО должны восстанавливаться водородом и окисью
углерода уже при 150° С; однако из-за малой скорости практически это достигается лишь около 450° С, либо в водных растворах.
Сульфид меди (II)
Сульфид меди (II), если его нагревать в нейтральной среде, разлагается по реакции:
4СuS → 2Cu2S + S2.
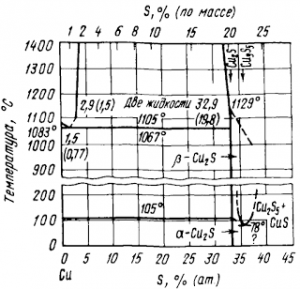
Сульфид Cu2S плавится при 1129° С и дает с медью эвтектику (1067°С).
Сплавы, более богатые серой, выше 1105°С расслаиваются на два насыщенных раствора, состав которых мало изменяется с повышением температуры (рис. 2).
Растворимость серы в твердой меди очень мала, при обычных температурах она менее 0,001%.
Скопление Cu2О и Cu2S на границах зерен во время кристаллизации металла, загрязненного кислородом и серой, уменьшает пластичность меди, которая в чистом виде весьма ковка, легко поддается волочению и прокатке в тонкую проволоку или фольгу.
Последняя при малой толщине просвечивается и кажется голубовато-зеленой.
Рис. 2. Диаграмма состояния системы Cu—S.
Растворимость меди с переходными металлами
Жидкая и твердая медь хорошо растворяют сходные с ней по группе периодической системы и кристаллической структуре переходные металлы 5-го и 6-го периодов — серебро и золото c жидкой медью оба они смешиваются в любых отношениях.
Золото и при обычных температурах дает непрерывный ряд твердых растворов, а растворимость серебра в меди при этом менее 0,1 % (по массе).
Статья на тему Свойства меди

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.