Простые сульфиды это минералы, сложные неорганические вещества, в состав которого всегда входит сера S, отсюда и название сульфиды.
Структурное строение у сульфидов построены из одиночных атомов или ионов серы или ее аналогов — селена или теллура.
Структура сульфидов еще недостаточно изучена и теория строения сульфидов и их систематика еще ждет своего исследователя.
Всю обширную группу сульфидов и их аналогов можно подразделить на подгруппы:
1) простых и сложных сульфидов;
2) дисульфидов простых и смешанных.
Примером сульфидов могут служить пирротин, сфалерит, галенит и другие.

Содержание страницы
Что такое простые сульфиды
Исключительно важную практическую роль в народном хозяйстве играют сернистые соединения тяжелых металлов.
Они представлены весьма значительным количеством минералов и уступают в этом отношении только силикатам.
Не являясь минералами массового распространения (породообразующими), сульфиды представляют особый интерес, как руды цветных металлов и часто как носители золота.
Со стороны физических свойств для них характерен металлический, реже алмазовидный блеск. Твердость их небольшая, за исключением лишь некоторых (пирит, арсенопирит).
Большинство сульфидов образуется из гидротермальных растворов различных температур. Но встречаются сульфиды, кристаллизующиеся непосредственно из магмы и ее летучих возгонов.
Кроме образования сульфидов в виде кристаллов, нередко можно видеть, что выпадение вещества шло первоначально в коллоидном состоянии и лишь впоследствии произошла раскристаллизация (колломорфная структура).
Возможно образование сульфидов и из холодных растворов или за счет осаждения тяжелых металлов сероводородом, или путем восстановления сернокислых растворов.
На земной поверхности сульфиды окисляются и переходят в сульфаты, карбонаты, окислы и другие соединения.
В структурном отношении сульфиды обычно построены из одиночных атомов или ионов серы или ее аналогов — селена или теллура, а также сходных с ней по роли мышьяка и сурьмы.
При этом указанные атомы заполняют по возможности полностью пространство, образуя плотнейшие упаковки.
Остальные элементы располагаются в свободных промежутках между ионами или атомами плотнейшей упаковки.
В некоторых случаях закономерность заполнения промежутков нарушается и некоторые пустоты оказываются незаселенными.
Такое «дефицитное» строение наблюдается у пирротина (Fex-1Sx), что объясняется тем, что не все ионы железа имеют валентность два.
А среди таковых встречаются также и трехвалентные, что естественно нарушает простоту формулы.
В некоторых сульфидах (MoS2) валентности полностью насыщаются уже в плоскостной группировке и получающиеся вследствие этого бесконечные-листы.
Между собой связываются лишь остаточными молекулярными связями, что ведет к образованию совершенной спайности по грани пинакоида (как у графита).
Ионы, заполняющие промежутки плотнейшей упаковки, могут принадлежать одному элементу (простые сульфиды) или нескольким разным элементам (сложные сульфиды).
Образование комплексных групп типа анионов не до казано и рассмотрение сложных сульфидов как сульфосолей не обосновано фактическими соотношениями в решетках сульфидов.
Можно лишь указать, что в некоторых сульфидах констатируется наличие молекулярных группировок, S2 или их аналогов. Этот факт позволяет выделить подгруппу дисульфидов (например, пирит FeS2).
Отмечаются и такие структуры сульфидов, в которых присутствуют как одиночные, так и сдвоенные сульфогруппы (ковеллин Cu2S · CuS2 = 3CuS).
Халькозин (медный блеск)
Химический состав халькозина — Cu2S. Часто — примесь железа и серебра. Тв. 2,5. Уд. в. 5,5—5,8. Сингония ромбическая.
Цвет черновато-свинцово-серый, матовый. Блеск слабый, полуметаллический. Встречается сплошными массами и вкрапленным в породу. Иногда образует кристаллы, имеющие вид шестигранных таблиц.
Диагностика, как определить. Халькозин отличается тусклым полуметаллическим блеском; режется ножом, причем получается блестящая поверхность разреза.
Встречается обычно в плотных агрегатах. Часто сопровождается зелеными примазками и налетами малахита.
Халькозин сходен с блеклыми рудами, от которых он отличается некоторой ковкостью, тогда как блеклые руды очень хрупки.
Халькозин образуется в верхних частях рудных жил в зоне вторичного обогащения при разложении медного колчедана и» блеклых медных руд.
Кроме того, встречается в песчаниках, образуясь из проникающих в них растворов медного купороса при содействии органических веществ.
Халькозин — очень ценная, достаточно распространенная богатая медиан руда, имеющая большое экономическое значение.
85% ежегодной мировой выплавки меди дают сернистые медные-руды, причем значительная часть приходится на халькозин, главным образом и топах цементации медных порфировых руд.
Применение. Очень богатая медная руда.
Цинковая обманка (сфалерит)
Химический состав сфалерита —ZnS. Постоянна примесь железа, доходящая до 22%; в этом случае-минерал принимает черный цвет и носит название марматита.
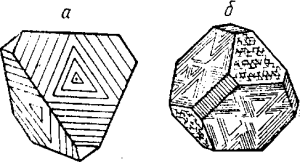
Часто содержит примесь Мn, иногда Cd, ln и др.Тв. 3,5. Уд, в. 3,9—4,2. Сингония кубическая (рис., а и б).
Название «цинковая обманка» дано немецкими рудокопами, так как из этого минерала, несмотря на сходство его с другими рудами, высокий удельный вес, долго не могли выплавить никакого металла.
Цинковая обманка — от темнобурого до желтого цвета. Редко бесцветная (клейофан). Обладает алмазным, иногда полуметаллическим блеском.
Спайность весьма совершенная. Кристаллы встречаются очень часто. Характерны двойники
Нередко встречается также в виде сплошных зернистых масс с кварцем, галенитом, пиритом и халькопиритом (полиметаллические руды).
Диагностика, как определить. Цинковая обманка отличается от других минералов алмазным или полуметаллическим блеском, совершенной спайностью и парагенезисом с сульфидами.
Па фарфоровой пластинке дает желтую или бурую черту различных оттенков (в зависимости от содержания железа), а галенит — черную черту.
Цинковая обманка образуется главным образом в рудных жилах и на контактах, из горячих водных растворов.
При окислении превращается в сульфаты цинка, а затем в труднорастворимые смитсонит и каламин.
Применение. Важнейшая цинковая руда. Обычно вместе с сфалеритом, но при несколько более низких температурах, образуется важнейшая свинцовая руда:
Свинцовый блеск (галенит)
Химический состав галенита — PbS. Часто содержит серебро, иногда до 5%. Тв. 2,5 Уд. в. 7,4—7,6. Сингония кубическая.
Серебросодержащий галенит является рудой на свинец и серебро: последнее извлекается попутно при выплавке свинца.
Цвет свинцово-серый. Блеск металлический. Встречается зернистыми плотными массами; часто в кристаллах, иногда хорошо образованных, в виде кубов и других форм кубической сингонии.
Отличается совершенной спайностью, по которой при ударе легко распадается на мелкие кубики (рис. 26).
Диагностика, как определить. Для свинцового блеска характерны: изометрический облик кристаллов (длина, ширина и высота кристаллов приблизительно равны между собою), совершенная спайность по кубу, весьма большой удельный вес.
От сходного сурьмяного блеска галенит можно отличить но большей твердости (не чертится ногтем) и по виду кристаллоид.
Чаще всего галенит образуется, отлагаясь вместе с кварцем, цинковой обманкой и другими сульфидами.
А также с карбонатами и флюоритом из горячих полных растворов по трещинам горных пород, давая таким образом жильные месторождения.
В зоне окисления переходит в сульфат (англезш) и карбонат (церуссит) и ряд других более сложных соединении.
Применение. Важнейшая руда на свинец и серебро.
Пирротин (магнитный колчедан)
Химический состав пирротина — Fex-1Sx Чисто содержит примеси никеля и кобальта. Тв. 3,5—4,5. Уд. в. 4,6. Сингония гексагональная.
Кристаллы встречаются редко. Бронзово-желтого цвета с красноватым оттенком. Магнитен (действует на магнитную стрелку).
Диагностика, как определить. Пирротин отличается от сходных с ним минералов (пирита, халькопирита) магнитностью (действует на магнитную стрелку) и характерным бронзовым цветом с красноватым оттенком.
Обычно встречается в зернистых плотных скоплениях, в рудных жилах и в горных породах основного типа и в контактовых типа скарнов. На поверхности неустойчив.
В СНГ пирротин известен на Кавказе (Садонский рудник). Пирротин, содержащий никель, примеси меди и платины, добывается в различных месторождениях, как руда никеля и платины.
Применение. В случае нахождения больших залежей применяется, как сырье для получения серной кислоты. Пирротин, содержащий никель,— важнейшая никелевая руда (Сэдбёри в Канаде).
Характерную группу сульфидов представляют собой сульфиды ртути, сурьмы и мышьяка.
Эти минералы, важные руды Hg, Sb и As, нередко встречаются вместе и представляют собою выделения наиболее низкотемпературных гидротермальных растворов.
Киноварь
Химический состав киновари: HgS. Обычно с примесью глины (печенковая руда). Тв. 2—2,5. Уд. в. 8—8,2. Сингония гексагональная.
Цвет малиновокрасиый. Блеск от алмазного до металлического.
Диагностика, как определить. Киноварь легко отличить от других минералов по красному цвету и черте, алмазному блеску кристаллов, малой твердости, весьма большому удельному весу и парагенезису с сурьмяным блеском.
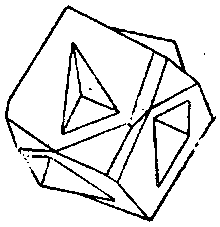
Киноварь похожа на кристаллический куприт, от которого отличается по облику кристаллов у киновари—двойники прорастания, у куприта — октаэдры) и по цвету черты.
Она встречается обычно в виде примазок, вкраплений и плотных масс, двойников прорастания (рис. 2) и мелких кристаллов в песчаниках и углистых сланцах; выделяется из горячих водных растворов.
В некоторых горячих источниках (Калифорния) киноварь выделяется и в настоящее время вместе с кремнеземом и пиритом. На поверхности очень стойка, иногда скопляется в россыпях.
Месторождения киновари мирового значения — Альмаден (Испания).
Применение, Единственная ртутная руда. Ценная красная краска для живописи.
Статья на тему простые сульфиды

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.