Расчеты по формулам
Прежде всего она непосредственно показывает, из каких элементов состоит данное вещество и сколько атомов каждого элемента содержит его молекула. Затем она позволяет рассчитать ряд величин, характеризующих данное вещество. Укажем важнейшие из этих расчетов.
1. Молекулярный вес вещества. Вычисляется по формуле как сумма весов атомов, входящих в состав молекулы вещества. О точности найденного таким образом молекулярного веса уже сказано в предыдущем статье.
2. Весовой состав сложного вещества. Состав всякого вещества может быть выражен отношением весовых количеств содержащихся в нем элементов. Это отношение прямо вытекает из формулы вещества.
Например, из формулы соды Na2СО3 видно, что в ней на два атома натрия приходится один атом углерода и три атома кислорода. Так как атомный вес натрия 23, углерода 12 и кислорода 16, то отношение между весовыми количествами этих элементов в любом количестве соды должно равняться:
23.2 : 12 : 16.3 = 46 : 12 : 48
Так же легко рассчитать по формуле и процентное содержание каждого элемента в данном веществе.
3. Плотность вещества в газообразном состоянии. Расчет производится по формуле
где D — плотность вещества, М — его молекулярный вес и M1 — молекулярный вес газа, по отношению к которому определяется плотность.
4. Вес 1 л газа при 0° и 760 мм давления. Граммолекула любого газа при нормальных условиях занимает объем 22,4 л, следовательно, вес (g) 1 л газа при тех же условиях будет равняться грамм молекулярному весу (М), деленному на 22,4:
5. Объем, занимаемый любым количеством газа. Если газ взят при 0° и 760 мм давления, то расчет проще всего произвести, исходя из величины грамм молекулярного объема.
Если же газ находится при иных условиях давления и температуры, то вычисление объема производится по уравнению:
По этому же уравнению легко рассчитать вес любого объема газа при данных условиях.
Статья на тему Расчеты по формулам


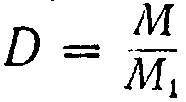
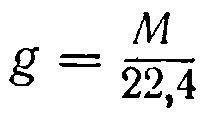
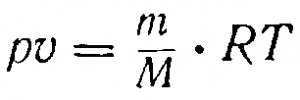
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.