Надсерная кислота H2S2O8
При пропускании электрического тока через 50%-ный раствор серной кислоты на катоде выделяется водород.
А на аноде ионы HSO4‘, теряя свои заряды, соединяются попарно и образуют надсерную кислоту H2S2O8:
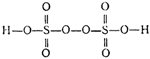
Рис. Строение надсерной кислоты.
2HSO4‘ — 2е—= H2S2O8
Надсерная кислота является производным перекиси водорода и промежуточным продуктом при получении последней электрохимическим путем.
Как и в перекиси водорода, два атома кислорода связаны здесь ковалентной связью, образуя «цепочку», характерную для перекисей.
Такие кислоты получили общее название надкислот и, кроме серы, известны для ряда других элементов.
Изучением надкислот много занимался академик Л. В. Писаржевский, которому химия обязана классическими исследованиями в этой области.
Все надкислоты благодаря наличию в их молекулах перекисной цепочки обладают, подобно перекисям, сильными окислительными свойствами.
Соли надсерной кислоты — персульфаты — применяются для некоторых технических целей и как средство для отбелки.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.