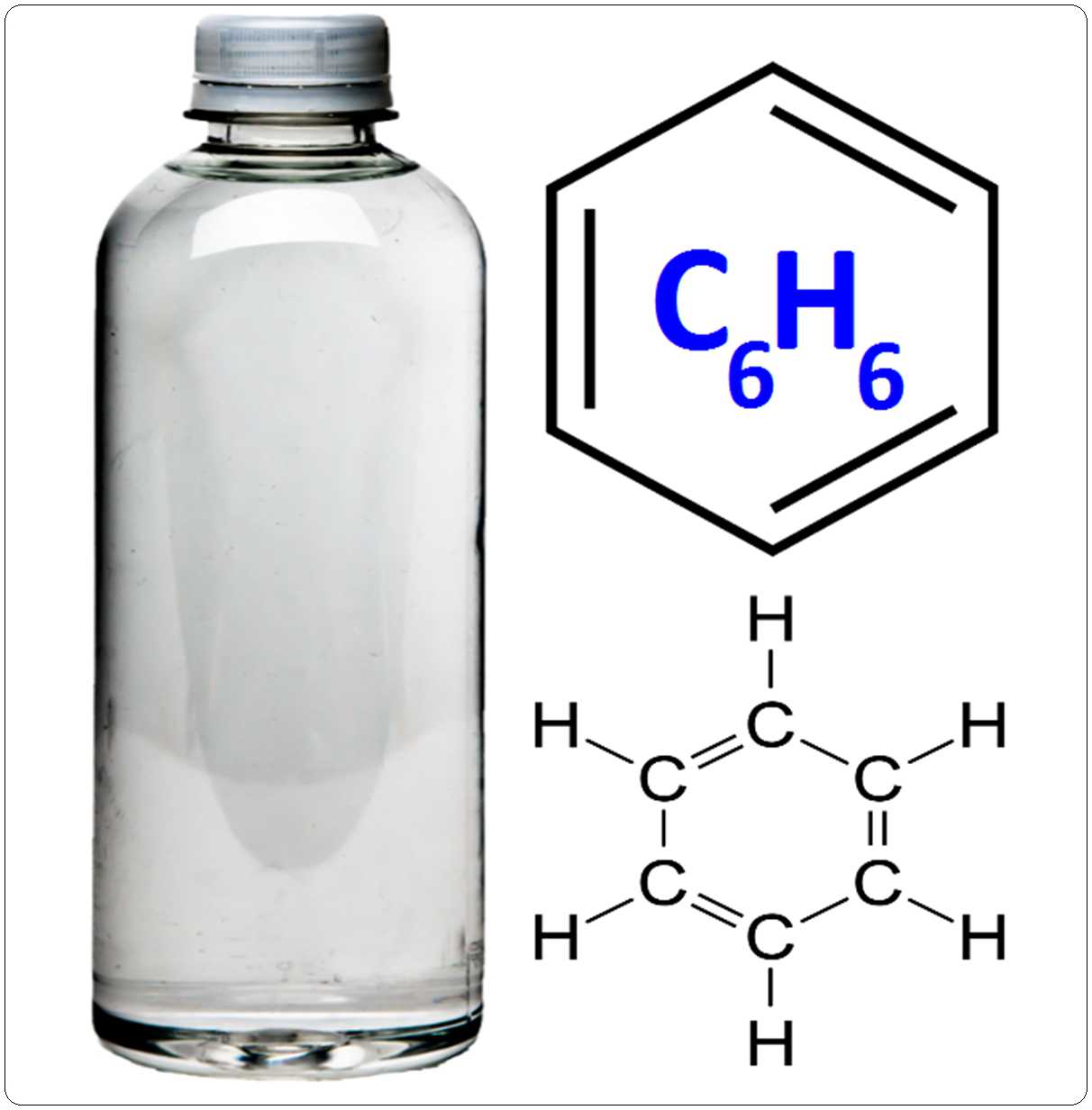
Бензол ароматический органический углеводород с формулой C6H6. Он является исходным соединением многих ароматических соединений.
Присутствие бензола можно распознать по его характерному запаху.
Содержание страницы
- 1. Что такое бензол
- 1.1. История
- 1.2. Физические свойства бензола
- 1.3. Химические свойства
- 1.4. Резонанс структур в бензоле
- 1.5. Получение бензола
- 1.6. Применение
- 1.7. О бензоле
- 1.8. Часто задаваемые вопросы и ответы?
Что такое бензол
Бензол имеет циклическую структуру с 6 атомами углерода и 6 атомами водорода. Каждый атом углерода связан с одним атомом водорода и двумя другими атомами углерода.
Из-за делокализации шести электронов в бензоле, на самом деле в бензоле нет отчетливой одинарной или двойной связи. Вот почему длина связи равна 1.39А.
Эти 6 электронов образуют электронные облака над и под ароматическим кольцом.
Бензол представляет собой замкнутое кольцо из шести атомов углерода, соединенных связями, которые чередуются между одинарными и двойными связями.
Каждый атом углерода ограничен одним атомом водорода.
Бензол и его производные являются важными компонентами важного химического сообщества, известного как ароматические соединения.
Является прекурсором при производстве масел, пластмасс, синтетики, каучука, красителей и лекарств.
Гидрирование соединения происходит гораздо медленнее по сравнению с гидрированием других органических соединений, которые содержат двойные связи углерод-углерод, и окислять бензол становится труднее, чем алкены.
Большинство реакций с бензолом относятся к определенному классу, который называется электрофильным ароматическим замещением.
Который в конечном итоге оставляет кольцо нетронутым, но замещается одним из атомов водорода, которые присоединены к нему.
Эти реакции обычно используются для получения производных бензола и являются универсальными по своей природе.
История
Бензол был открыт великим английским физиком Майклом Фарадеем в 1825 году, а бензол стал доступен в больших количествах в 1842 году.
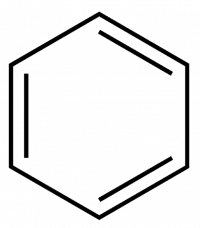
Первая наиболее удачная структурная формула бензола была предложена в 1865 г. немецким-химиком Кекуле.
Согласно его представлениям в молекуле бензола чередуются двойные и одинарные связи между атомами углерода, замкнутыми в шестичленный цикл (рис.1).
Эта формула показывает равноценность всех атомов углерода и водорода, которые входят в молекулу бензола, что было доказано экспериментально.
Интересный факт:он очень быстро испаряется в воздухе. Его пар тяжелее воздуха и может опускаться в низины.
Физические свойства бензола
Бензол-бесцветная жидкость; имеющая характерный запах. Легко переходит в твердое состояние: температура плавления бензола составляет +5,5 °с, температура кипения +80.1 °с.
Имеет ароматический запах и представляет собой бесцветную жидкость.
В воде бензол практически не растворяется, при взбалтывании образует с ней азеотропную смесь с температурой кипения 69,25 °C (при 91 % бензола), но является хорошим растворителем многих органических веществ.
Как многие углеводороды легче воды.
Он легко воспламеняется и летуч. Имеет плотность 0,87 г/см3.
Бензол может проявлять резонанс. Бензол легко воспламеняется и может даже гореть с помощью пламени самокрутки.
Химические свойства
Химические свойства бензола и других ароматических соединений характеризуются рядом особенностей.
Бензол характеризуется реакциями замещения атомов водорода в бензольном кольце.
Эти реакции происходят по механизму электрофильного замещения.
Электрофильная частица X+ («любящая электроны», обычно положительная заряженная) взаимодействует с π.
Электронами молекулы бензола, образуя π-комплекс, который переходит в σ-комплекс.
В σ-комплексе частица соединена с одним из атомов углерода, в результате ароматический характер молекулы нарушается.
Далее от σ-комплекса отщепляется протон и восстанавливается ароматический характер ядра.
Бензол проявляет следующие химические реакции: нитрование, сульфирование, галогенирование и другие.
Нитрование
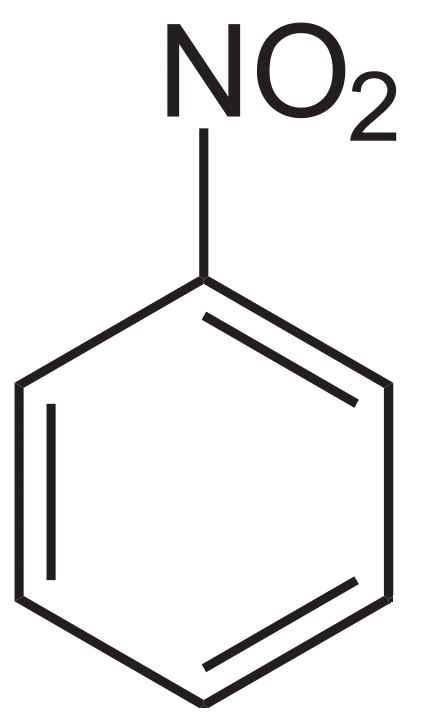
При воздействии на бензол нитрирующей смеси (Смесь концентрированных азотной и серной кислот) происходит замещение водорода в ядре бензола на группу NО2; этот процесс называется нитрованием.
Бензол вступает в реакцию с азотной кислотой в присутствии серной кислоты при 55°C и образует нитробензол.
Реакция нитрования:
C6H6 + HNO3 (катализатор H2SO4) → C6H5NO2 + H2O
Реакция происходит по механизму электрофильного замещения. Роль электрофильной частицы играет Ион NО2+, который образуется в результате реакции:
HNO3 + H2SO4 ⇄ NO2+ + H2O + HSO4—
Сульфирование
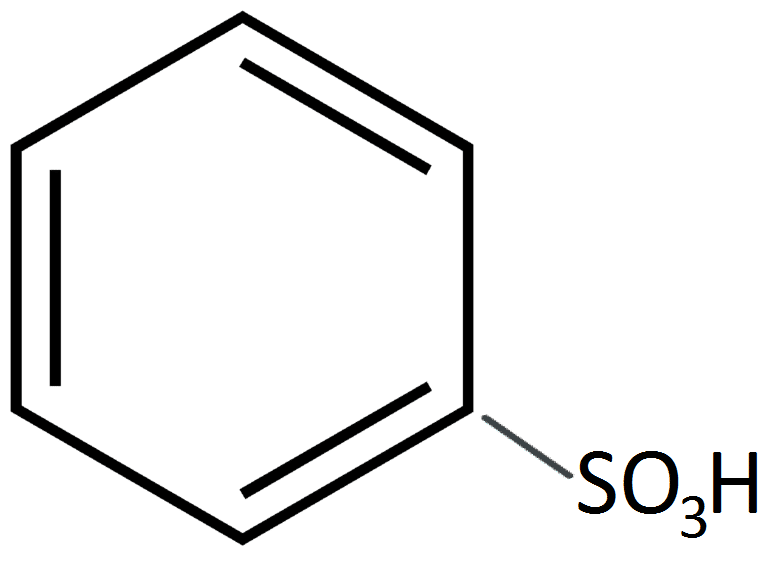
Водород в бензольном ядре может быть замещен на сульфогруппу ЅО3Н под действием концентрированной серной кислоты; этот процесс называется сульфированием.
Бензол нагревают с дымящейся серной кислотой H2SO4 и получают бензолсульфоновую кислоту.
Реакция сульфирования:
C6H6 + H2SO4 → C6H5(HSO3) + H2O
Галогенирование
В присутствии кислоты Льюиса бензол вступает в реакцию с галогеном с образованием арилгалогенида.
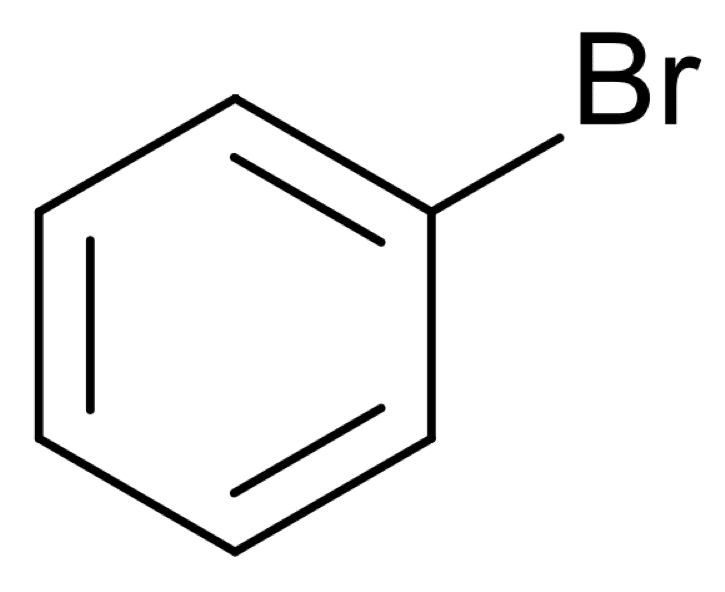
Замещение водорода в бензольном ядре на хлор или бром осуществляется при взаимодействии бензола с галогенами с участием катализатора.
Реакцию могут катализировали FеСl3 (или FеВr3) и АlСl3, при этом образуются различные продукты.
Реакция галогенирования:
C6H6 + Br2 (катализатор FеВr3) → C6H5Br + HBr
Алкилирование
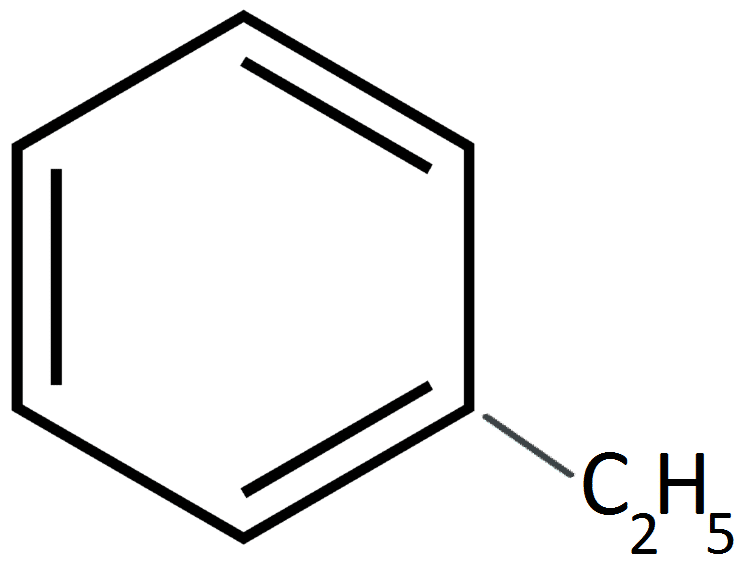
В молекулу бензола вместо водорода можно ввести алкильный радикал.
Процесс алкилирования можно осуществить действием на бензол галогенопроизводной алкана или олефина при наличии катализатора (хлорид алюминия АlСl3).
Реакция алкилирования:
C6H6 + С2Н4 → C6H10
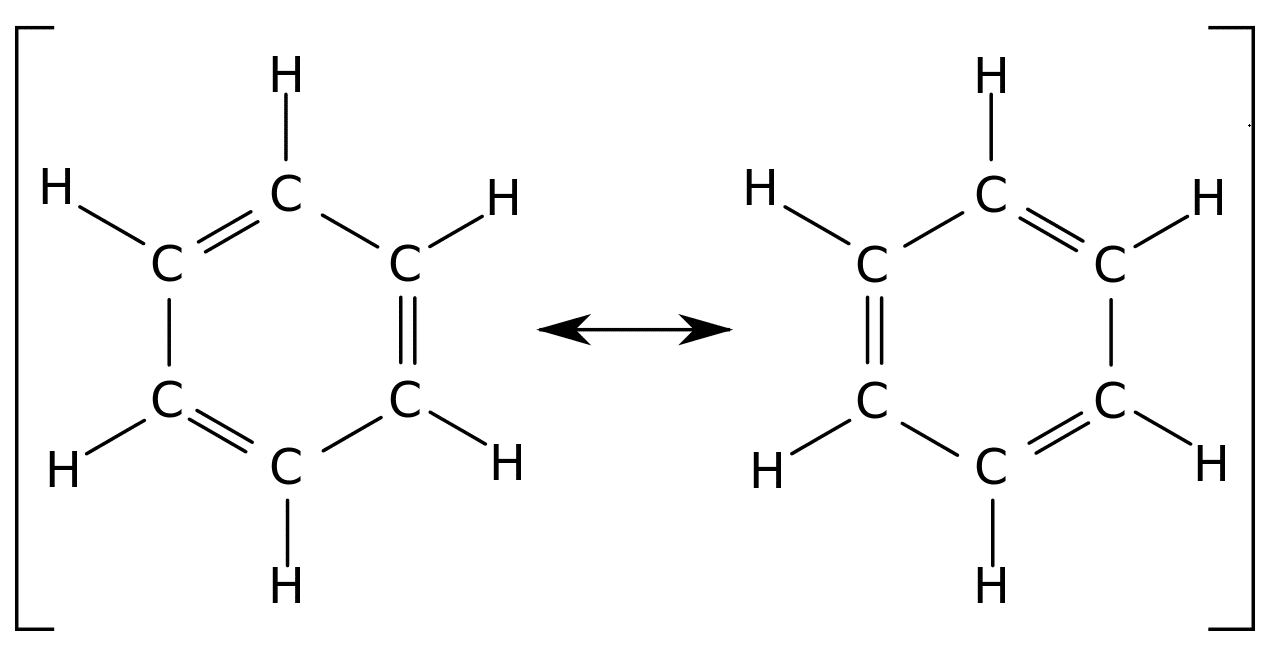
Резонанс структур в бензоле
Резонансная форма соединения это не что иное, как другой способ представления точечной структуры этого соединения Льюиса.
Бензол демонстрирует резонанс, поскольку у него есть более чем один способ размещения двойных связей в кольце. Бензол имеет 2 резонирующие структуры.
Резонансные формы или резонирующие структуры отличаются только расположением электронов.
Резонансная структура бензола отличается только расположением электронов, а количество атомов углерода и атомов водорода в бензоле остается прежним.
Двойные связи, присутствующие в бензоле, вращаются в резонирующих структурах бензола и обеспечивают стабильность бензола. Резонансная структура показывает возможные структуры соединения.
Гибридная структура бензола более стабильна, чем резонансные структуры бензола, поскольку обладает меньшей энергией, чем резонирующие структуры бензола.
Интересный факт: образуется как в результате естественных процессов, так и в результате деятельности человека.
Получение бензола
Из алкинов – этин пропускают через раскаленную докрасна железную трубку при температуре 873 К, он проходит полимеризацию и образует бензол.
Декарбоксилирование ароматических кислот. Бензоат натрия нагревают с гидроксидом натрия в присутствии оксида кальция с получением бензола.
Восстановление фенола – Фенол нагревают с цинком с получением бензола.
Применение
Бензол важным сырьем для органического синтеза, его используют при извлечении многих других ароматических соединений.
Применяют в производстве красителей, пластмасс, пестицидов, взрывчатых веществ, лекарств; его используют как растворитель лаков, красок.
Входит в состав топлива, которое используется в двигателях внутреннего сгорания.
Используется при получении полистирола.
В производстве фенола.
При приготовлении анилина и моющих средств.
В производстве нейлоновых волокон.
Он используется в качестве растворителя органических соединений при получении многих полезных соединений.
О бензоле
1. Считается одним из важнейших органических соединений, имеющих химическую формулу C6H6.
2. Считается исходным соединением многих ароматических соединений.
3. Является одним из простейших органических соединений и ароматических углеводородов.
4. Является одним из элементарных продуктов нефтехимии и одним из природных компонентов сырой нефти. Он имеет запах бензина и представляет собой бесцветную жидкость.
5. Один из высокотоксичных соединений и канцерогенен по своей природе. В основном он используется в производстве полистирола.
6. Считается одним из природных веществ, образующихся в результате извержения вулканов и лесных пожаров.
7. Присутствует во многих растениях и животных, но бензол также является одним из основных промышленных химических веществ, производимых из угля и нефти.
8. Представляет собой прозрачную и бесцветную жидкость, поскольку является чистым химическим веществом.
9. Используется для производства других химических веществ наряду с другими типами пластмасс, пестицидами и моющими средствами.
Часто задаваемые вопросы и ответы?
Это химическое соединение органического происхождения, которое представляет собой жидкость без цвета и специфическим сладковатым запахом.
В химии относят к простейшим ароматическим углеводородам.
Фениловый водород, бензен.
В результате переработки нефти и каменного угля. Кроме того, бензол может быть получен по реакции циклотримеризации ацетилена.