Fe железо (Ferrum) — химический элемент 8-й группы, с порядковым номером 26 в периодической системе.
Находится в четвертом периоде. Температура плавления: 1535 ℃, температура кипения 2880° С. Плотность: 7.87 г/см3.
Атомный номер 26, атомная масса 55,847.
Его кристаллические модификации:
- Альфа.
- Гамма.
- Дельта-железо.
Содержание страницы
Электронная формула
Полная электронная формула атома железа в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d6 4s2
Сокращенная электронная конфигурация Fe:
[Ar] 3d6 4s2
Электронная формула атома железа в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d6
Электронно-графическая схема железа (Fe)
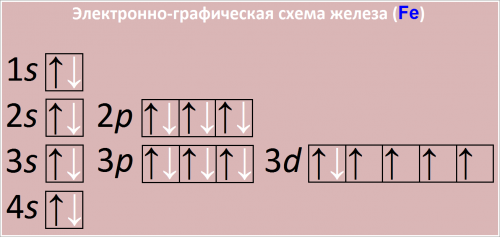
Рис. Схема распределения электронов по атомным орбиталям в атоме железа.
Энергетические уровни
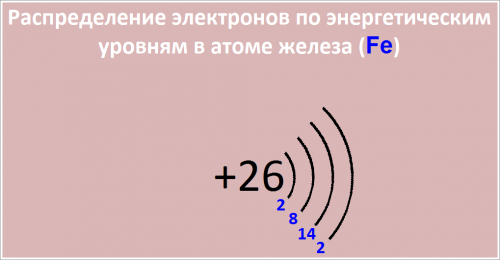
Распределение электронов по энергетическим уровням в атоме Fe:
1-й уровень (K): 2
2-й уровень (L): 8
3-й уровень (M): 14
4-й уровень (N): 2
Рис. Распределение электронов по энергетическим уровням в атоме железа Fe.
Валентные электроны железа
Количество валентных электронов в атоме железа — 8.
Таблица квантовых чисел железа (N — главное, L — орбитальное, M — магнитное, S — спин).
| Орбиталь | N | L | M | S |
| s | 4 | 0 | 0 | +1/2 |
| s | 4 | 0 | 0 | -1/2 |
| d | 3 | 2 | -2 | +1/2 |
| d | 3 | 2 | -1 | +1/2 |
| d | 3 | 2 | 0 | +1/2 |
| d | 3 | 2 | 1 | +1/2 |
| d | 3 | 2 | 2 | +1/2 |
| d | 3 | 2 | -2 | -1/2 |
В соединениях железо проявляет степень окисления: +1 +2 +3 +4 +5 +6 .
Стабильные изотопы
|
Изотоп
|
Протоны
|
Нейтроны
|
Атомная масса изотопа
|
|
54Fe
|
26
|
28
|
~53.9396105
|
|
56Fe
|
26
|
30
|
~55.9349375
|
|
57Fe
|
26
|
31
|
~56.935394
|
|
58Fe
|
26
|
32
|
~57.9332756
|
Природное железо состоит из стабильных изотопов: 54Fe (5,84%), 56Fe (91,68%), 57Fe (2,17%) и 58Fe (0,31%).
Получены радиоактивные изотопы 52Fe, 53Fe, 56Fe, 59Fe и 60Fe с периодами полураспада соответственно 8,3 ч, 8,9 мин 2,9 года, 45 дней и 8,4 ч.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.