Теория:
Степень окисления нихония (Nh) в химических соединениях наиболее вероятно проявляет стабильные значения +1 и +3.
Это обусловлено положением элемента в 13-й группе Периодической системы (подгруппа бора), где он является тяжелым аналогом таллия (Tl).
Из-за релятивистских эффектов состояние +1 для него может быть даже более характерным, чем для его соседей по группе.
Кроме того, выделяют показатель 0, который относится к нихонию в виде простого вещества (тяжелый радиоактивный металл).
Например для предполагаемой стабильной СО +1: в соединении NhCl (хлорид нихония I) или NhOH (гидроксид нихония I) заряд иона равен +1.
В этом состоянии нихоний ведет себя как «сверхтяжелый» аналог таллия.
Для сравнения, другие СО: состояние +3 (например, в NhCl3) также предсказывается теорией.
Но оно может быть менее устойчивым из-за эффекта «инертной электронной пары», который максимально выражен у элементов конца 7-го периода.
- Почему +1 и +3? Электронная формула нихония [Rn] 5f14 6d10 7s2 7p1 предполагает отдачу либо одного 7p-электрона (СО +1), либо трех электронов с внешнего уровня (СО +3).
- Почему +1 может быть стабильнее? Релятивистское сжатие 7s-орбитали делает эти электроны очень труднодоступными для химических реакций, поэтому нихоний «предпочитает» отдавать только один p-электрон.
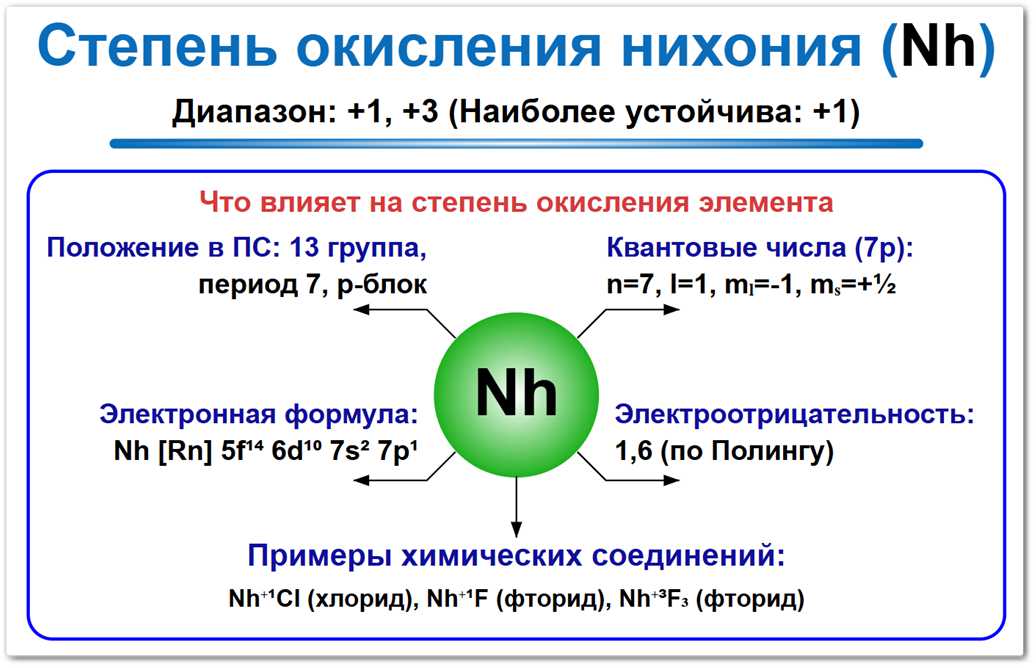
Рис. 1. Основные степени окисления нихония: 0, +1 и +3.
В настоящее время химические свойства нихония изучаются экспериментально в основном в газовой фазе, где подтверждается его высокая летучесть и склонность к низким степеням окисления.
Важно заметить, что нихоний — крайне короткоживущий элемент. Самые стабильные изотопы живут всего несколько секунд.
Его название происходит от японского слова «Нихон» (Япония), так как элемент был впервые синтезирован учеными из института RIKEN.
Релятивистские эффекты делают нихоний химически менее активным, чем таллий, сближая его свойства по инертности с благородными газами (хотя он остается металлом).
Содержание страницы
- 1. Почему +1 — наиболее вероятная стабильная СО у нихония
- 2. Степень окисления нихония в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему нихоний выбирает заряд +1?
- 4. 4 способа определить степень окисления нихония
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления нихония
- 6. Шпаргалка
- 7. Нихоний вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +1 — наиболее вероятная стабильная СО у нихония
Стабильность определяется энергией отрыва электронов с сильно сжатых 7s и 7p уровней.
- В простом веществе (Nh0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d10 7s2 7p1. - В одновалентном ионе (Nh+1): Нихоний теряет один 7p-электрон. Конфигурация:
[Rn] 5f14 6d10 7s2.

Рис. 2. Схема образования степени окисления +1: удаление 7p-электрона.
Степень окисления нихония в соединениях
- Хлорид нихония(I) (NhCl): Nh +1.
- Гидроксид нихония(I) (NhOH): Nh +1.
- Хлорид нихония(III) (NhCl3): Nh +3.
Высшая степень окисления
Высшая степень окисления Nh теоретически равна +5 (при вовлечении d-электронов), но практически достижимой считается +3.
Низшая степень окисления
Характерна степень окисления 0 (атомарное состояние).
Промежуточные степени окисления
Наиболее важной промежуточной и одновременно стабильной является СО +1.
Важно: Нихоний — это первый элемент 13-й группы, у которого эффект инертной пары делает состояние +1 доминирующим над состоянием +3.
Почему нихоний выбирает заряд +1?
- Релятивистская стабилизация: 7s2-электроны слишком сильно притянуты к ядру, чтобы участвовать в образовании связей.
- Сходство с благородными металлами: В некоторых опытах нихоний проявляет инертность, схожую с золотом, предпочитая низкие заряды.
4 способа определить степень окисления нихония
По таблице Менделеева
- Семейство: Постпереходные металлы (p-элементы).
- Валентные электроны: 3 (но активен часто 1).
- Атомная масса: ~286 а.е.м.
По валентности (Число связей)
Валентность нихония (Nh) чаще всего равна I или III.
В отличие от бора или алюминия, он неохотно образует три связи, стремясь к монохромности (одной связи).
Детальные примеры:
- В NhCl: Нихоний образует одну ковалентную связь с хлором, проявляя валентность I.
- В гипотетическом Nh2O3: Нихоний проявляет валентность III, аналогично оксиду таллия.
По электронной конфигурации
Электронная формула нихония: [Rn] 5f14 6d10 7s2 7p1.
Как происходит ионизация:
- Валентные электроны: На внешнем слое 3 электрона (7s2 7p1).
- Механизм потери: Сначала уходит наиболее удаленный 7p-электрон (СО +1).
- Энергетический барьер: Для СО +3 нужно затратить гораздо больше энергии, чтобы «распарить» 7s-электроны.
По химическому соединению (Алгебраический расчет)
Пример для NhCl3:
- 1. Хлор (Cl) имеет СО -1.
- 2. 3 атома хлора дают суммарный заряд -3.
- 3. Уравнение для нихония (x): x + (-3) = 0.
- 4. Ответ: x = +3.
✅ Вывод: Степень окисления нихония в трихлориде равна +3.
Примеры степеней окисления нихония
| СО | Характеристика | Примеры |
|---|---|---|
| +1 | Наиболее характерная стабильная СО. | NhCl, NhOH |
| +3 | Возможная, но менее устойчивая. | NhCl3, NhF3 |
Шпаргалка
- +1 — самая устойчивая СО из-за релятивистских эффектов.
- Аналог таллия — ищите сходство в химии Tl+.
Нихоний вне учебника: что скрывает наука?
Химия золота и нихония:
Исследования по адсорбции нихония на золотых поверхностях показали, что он ведет себя почти как инертный газ или благородный металл.
Это подтверждает, что его СО 0 очень устойчива в атомарном виде.
Летучесть соединений:
Хлориды нихония крайне летучи. Это свойство используется для того, чтобы отделить его от других продуктов ядерных реакций в газовых анализаторах.
Амфотерность:
Предполагается, что гидроксид NhOH будет проявлять сильные основные свойства, подобно TlOH, что делает его уникальным среди сверхтяжелых металлов.
Пример решения задачи:
▶️ Дано:
Соединение: NhCl (хлорид нихония I).
⌕ Найти:
Определите степень окисления (СО) нихония.
✨ Решение:
1. Хлор в бинарных соединениях с металлами проявляет СО -1.
2. В молекуле 1 атом хлора, заряд -1.
3. Сумма зарядов должна быть 0: x + (-1) = 0.
4. x = +1.
✅ Ответ:
СО нихония (Nh) в данном хлориде равна +1.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: для 13-й группы СО +4 не характерна (типичны +1 и +3).
Часто задаваемые вопросы
Наиболее устойчивой для химии в растворах и твердых телах считается +1.
Ситуация с (Nh) аналогична коперницию, но со своими особенностями для 13-й группы:
1. Нихоний легко отдает один p-электрон, образуя устойчивую степень окисления +1.
2. При более жестких условиях он может задействовать инертную 7s2-пару, переходя в +3.
3. В экстремальных случаях могут вовлекаться даже электроны с 6d-подуровня, что теоретически допускает СО до +5.
Ему гораздо «выгоднее» избавляться от своих электронов, чем пытаться удержать чужие.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.