Теория:
Степень окисления мейтнерия (Mt) в химических соединениях на данный момент является предметом теоретических дискуссий, но наиболее предсказуемыми и стабильными считаются значения +3, +4 и +1.
Это обусловлено положением элемента в 9-й группе Периодической системы, где он является тяжелым аналогом иридия (Ir) и кобальта (Co).
Кроме того, выделяют показатель 0, который относится к мейтнерию в виде простого вещества (предположительно тяжелый металл платиновой группы).
Например для наиболее вероятной СО +3: в гипотетическом соединении MtCl3 (хлорид мейтнерия III) заряд иона равен +3.
В этом состоянии мейтнерий проявляет свойства, схожие с иридием.
Для сравнения, другие СО: теоретические расчеты показывают, что из-за сильных релятивистских эффектов мейтнерий может проявлять необычно высокую стабильность в более низких степенях окисления (+1).
Или, наоборот, достигать высоких значений (+6), характерных для платиноидов.
- Почему +3? Электронная формула мейтнерия [Rn] 5f14 6d7 7s2 предполагает возможность потери трех электронов (двух 7s и одного 6d) для формирования типичной для 9-й группы конфигурации.
- Почему другие СО вероятны? Сильное сжатие 7s-орбиталей и расширение 6d-орбиталей из-за скорости электронов меняет привычный порядок ионизации, делая мейтнерий уникальным d-элементом.
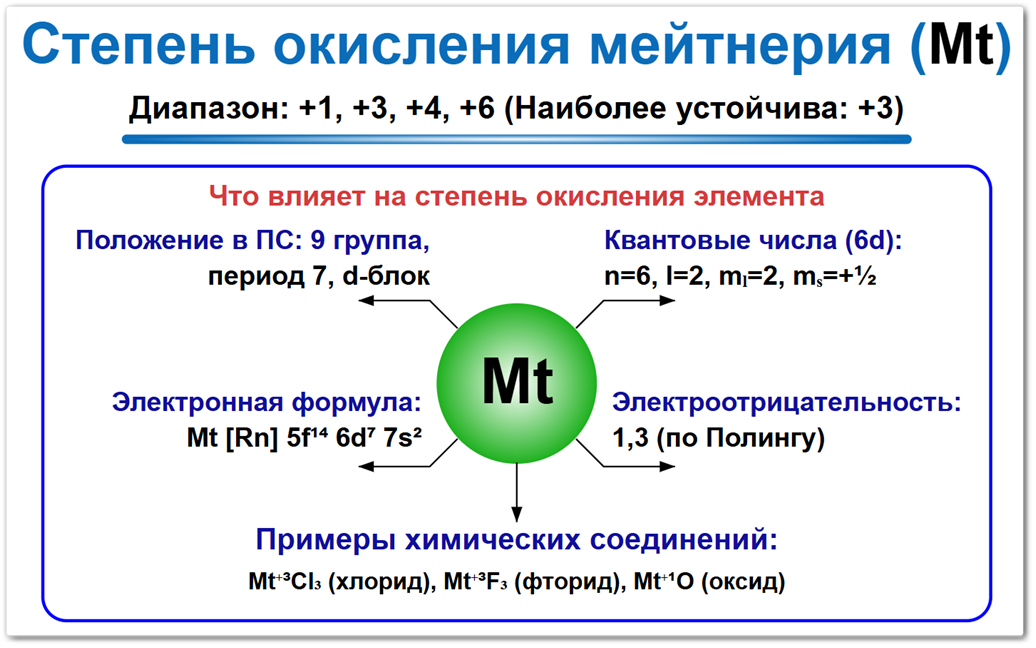
Рис. 1. Основные предполагаемые степени окисления мейтнерия: 0, +1 и +3.
Состояние +3 считается наиболее устойчивым в водных растворах (согласно расчетам), в то время как +1 может быть стабильным в газовой фазе.
Важно заметить, что мейтнерий — это «экстремально» радиоактивный элемент.
Он был впервые синтезирован в 1982 году, и с тех пор было получено лишь несколько десятков его атомов.
Его химия на данный момент почти полностью базируется на квантовохимических расчетах, так как период полураспада самых стабильных изотопов (Mt-278) составляет всего около 5-8 секунд.
Экспериментальное подтверждение его степеней окисления — это вызов для современной науки, требующий работы с «одним атомом за раз».
Содержание страницы
- 1. Почему степени окисления мейтнерия так сложно предсказать?
- 2. Степень окисления мейтнерия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему мейтнерий может вести себя необычно?
- 4. 4 способа определить степень окисления мейтнерия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления мейтнерия
- 6. Шпаргалка
- 7. Мейтнерий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему степени окисления мейтнерия так сложно предсказать?
Стабильность определяется балансом между энергией ионизации и релятивистским смещением уровней.
- В простом веществе (Mt0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d7 7s2. - В ионе (Mt+3): Мейтнерий теряет три электрона. Конфигурация:
[Rn] 5f14 6d6.

Рис. 2. Схема образования степеней окисления Mt: влияние релятивистской стабилизации 7s-оболочки.
Степень окисления мейтнерия в соединениях
- Мейтнерий металлический (Mt): Mt 0.
- Трифторид мейтнерия (MtF3): Mt +3 (прогноз).
- Гексафторид мейтнерия (MtF6): Mt +6 (возможная высшая СО).
Высшая степень окисления
Высшая степень окисления Mt теоретически может достигать +6 или даже +9 (по аналогии с иридием), но наиболее вероятный предел стабильности — +6.
Низшая степень окисления
Характерна степень окисления 0 или +1.
Промежуточные степени окисления
Считаются вероятными +4 и +2, однако они могут быть склонны к диспропорционированию.
Важно: Мейтнерий назван в честь физика Лизе Майтнер, одной из первооткрывательниц деления ядер. Это единственный элемент, названный исключительно в честь реальной женщины-ученого (Кюрий назван в честь обоих супругов).
Почему мейтнерий может вести себя необычно?
- Релятивистская химия: Из-за большой массы ядра электроны движутся так быстро, что 7s-орбиталь «сжимается» и становится очень химически инертной, что затрудняет достижение высоких СО.
- Сходство с благородными металлами: Ожидается, что мейтнерий будет очень благородным (химически пассивным) металлом, превосходя в этом даже платину и иридий.
4 способа определить степень окисления мейтнерия
По таблице Менделеева
- Семейство: Трансактиноиды (d-элементы).
- Валентные электроны: 9 (7 на 6d и 2 на 7s).
- Атомная масса: ~278 а.е.м. (для наиболее стабильного изотопа).
По валентности (Число связей)
Валентность мейтнерия (Mt) в прогнозируемых соединениях чаще всего принимается равной III или IV.
В комплексных соединениях он может проявлять высокие координационные числа (до 6), образуя октаэдрические комплексы.
По электронной конфигурации
Электронная формула мейтнерия: [Rn] 5f14 6d7 7s2.
Механизм ионизации:
- Стабильность 7s: Релятивистский эффект стабилизирует 7s-электроны, поэтому мейтнерий может неохотно их отдавать.
- Потеря электронов: Чаще всего предполагается уход d-электронов, что формирует степень окисления +3.
По химическому соединению (Алгебраический расчет)
Пример для гипотетического MtF3 (фторид мейтнерия III):
- 1. Фтор (F) — самый электроотрицательный элемент, СО = -1.
- 2. В молекуле 3 атома фтора: 3 · (-1) = -3.
- 3. Обозначим СО мейтнерия за x. Уравнение: x + (-3) = 0.
- 4. Решение: x = +3.
✅ Вывод: Степень окисления мейтнерия в этом соединении равна +3.
Примеры степеней окисления мейтнерия
| СО | Характеристика | Примеры |
|---|---|---|
| +3 | Наиболее вероятная стабильная СО. | MtF3 (прогноз) |
| +1 | Релятивистски стабильная СО. | MtCl (газ) |
Шпаргалка
- +3 — основная ожидаемая СО.
- Иридий — химический ориентир, но мейтнерий более инертен.
Мейтнерий вне учебника: что скрывает наука?
Золотистый блеск?
Хотя никто не видел мейтнерий в макроскопическом количестве, расчеты предсказывают, что из-за релятивистского сдвига энергетических уровней этот металл мог бы иметь цвет, отличный от серебристого (возможно, желтоватый или золотистый), подобно золоту.
Самый благородный из металлов:
Существует гипотеза, что мейтнерий может оказаться самым химически стойким элементом во всей таблице Менделеева, сопротивляясь воздействию даже самых сильных кислот-окислителей.
Химия в компьютерных моделях:
Поскольку мейтнерий распадается быстрее, чем можно провести обычную химическую реакцию, ученые используют суперкомпьютеры для моделирования его поведения в растворах кислот, предсказывая формы его существования как [MtCl6]3-.
Интересный факт: Название «мейтнерий» было предложено, чтобы восстановить историческую справедливость в отношении Лизе Майтнер, чья роль в открытии деления ядра долгое время замалчивалась Нобелевским комитетом.
Пример решения задачи:
▶️ Дано:
Соединение: MtF6 (предполагаемый гексафторид мейтнерия).
⌕ Найти:
Определите высшую степень окисления (СО) мейтнерия в этом соединении.
✨ Решение:
1. Фтор (F) всегда проявляет СО -1.
2. В молекуле 6 атомов фтора, их суммарный заряд: 6 · (-1) = -6.
3. Молекула нейтральна, значит заряд Mt должен быть x:
x + (-6) = 0 ⇒ x = +6.
✅ Ответ:
СО мейтнерия (Mt) в данном фториде равна +6.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: мейтнерий крайне нестабилен, его изотопы живут секунды.
Часто задаваемые вопросы
Большинство ученых склоняются к тому, что в обычных условиях наиболее устойчивым будет состояние +3.
У сверхтяжелых элементов, таких как мейтнерий (Mt), электроны на внешних орбиталях движутся с огромными скоростями.
Это приводит к двум последствиям: Стабилизация s-орбиталей: внешние электроны сильнее «прижимаются» к ядру.
Низкое сродство к электрону: атому крайне невыгодно принимать лишние электроны и удерживать их, чтобы образовать отрицательный заряд.
