Теория:
Степень окисления дубния (Db) в химических соединениях преимущественно проявляет значение +5.
Это обусловлено положением элемента в 5-й группе Периодической системы, где высшая степень окисления соответствует номеру группы и конфигурации валентных электронов.
Кроме того, выделяют показатель 0, который относится к дубнию в виде простого вещества (тяжелый радиоактивный металл).
Например для наиболее стабильной СО +5: в соединении DbCl5 (хлорид дубния V) или DbO2Cl (оксохлорид дубния) заряд иона равен +5.
В этом состоянии дубний является аналогом ниобия (Nb) и тантала (Ta).
Для сравнения, другие СО: попытки обнаружить иные степени окисления на текущем уровне развития экспериментальной техники ограничены.
Так как +5 является энергетически наиболее выгодной, хотя релятивистские эффекты могут стабилизировать более низкие состояния.
- Почему +5? Электронная формула дубния [Rn] 5f14 6d3 7s2 предполагает возможность отдачи пяти внешних электронов.
- Почему дубний особенный? Будучи трансактиноидом, он демонстрирует постепенный переход от химии актиноидов к химии d-переходных металлов, сохраняя при этом особенности «сверхтяжелой» химии.
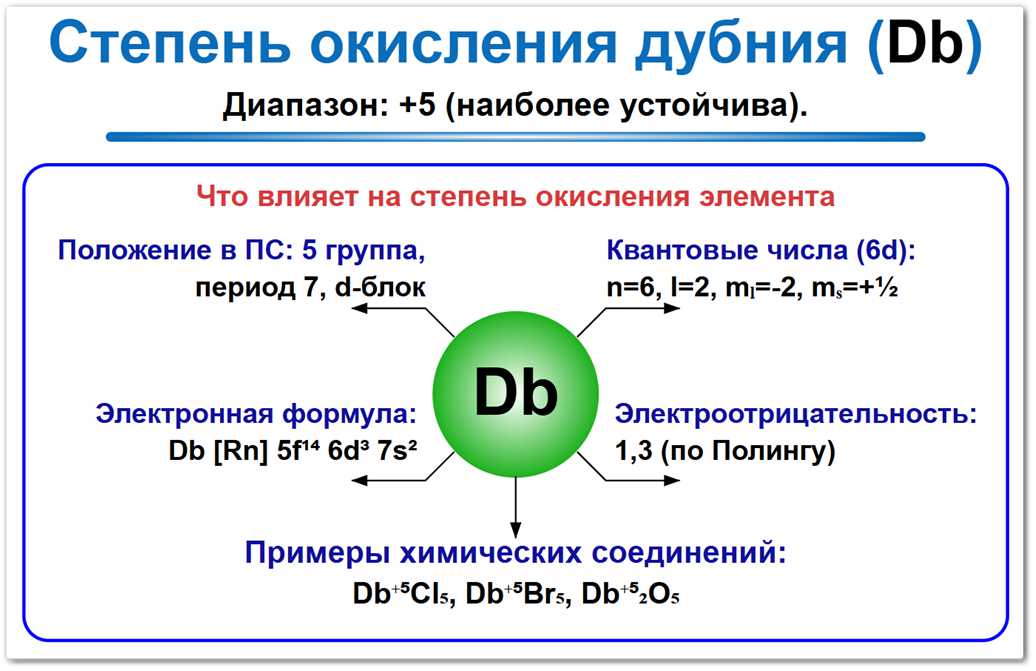
Рис. 1. Основная степень окисления дубния: 0 и +5.
Состояние +5 является наиболее устойчивым и единственным надежно зафиксированным в экспериментах по газофазной химии хлоридов дубния.
Важно заметить, что дубний — крайне радиоактивный элемент, синтезируемый на ускорителях тяжелых ионов.
Его изучение ведется методами «химии одного атома», что накладывает колоссальные ограничения на точность.
На свойства дубния сильно влияют релятивистские эффекты, которые делают его поведение схожим с танталом, но с заметными отличиями из-за деформации электронных орбиталей.
Содержание страницы
- 1. Почему +5 — самая устойчивая степень окисления у дубния
- 2. Степень окисления дубния в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему дубний предпочитает заряд +5?
- 4. 4 способа определить степень окисления дубния
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления дубния
- 6. Шпаргалка
- 7. Дубний вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +5 — самая устойчивая степень окисления у дубния
Стабильность определяется заполнением внешних оболочек и соответствием электронной структуре 5-й группы.
- В простом веществе (Db0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d3 7s2. - В пятивалентном ионе (Db+5): Дубний теряет 5 валентных электронов. Конфигурация:
[Rn] 5f14(стабильный инертный остов).

Рис. 2. Схема образования степени окисления +5: удаление 6d и 7s электронов.
Степень окисления дубния в соединениях
- Хлорид дубния(V) (DbCl5): Db +5.
- Оксохлорид дубния (DbO2Cl): Db +5.
Высшая степень окисления
Высшая степень окисления Db равна +5.
Низшая степень окисления
Характерна степень окисления 0 в металлическом состоянии.
Промежуточные степени окисления
Данные о других стабильных СО ограничены, +5 остается доминирующей.
Важно: Дубний назван в честь города Дубна, центра ядерных исследований, что подчеркивает вклад советских ученых в открытие этого элемента.
Почему дубний предпочитает заряд +5?
- Групповая принадлежность: Подобно ванадию, ниобию и танталу, он стремится к 5-валентному состоянию.
- Электронная конфигурация: Потеря 5 электронов доводит его до конфигурации [Rn]5f14, что энергетически наиболее выгодно.
4 способа определить степень окисления дубния
По таблице Менделеева
- Семейство: Трансактиноиды (d-элементы).
- Валентные электроны: 5.
- Атомная масса: ~268 а.е.м.
По валентности (Число связей)
Валентность дубния (Db) стабильно равна V. Это аналог тантала, проявляющий характерные для этой группы связи.
- В DbCl5: Атом Db связан с пятью атомами хлора.
- В DbO2Cl: Сложное соединение, где Db сохраняет валентность V.
По электронной конфигурации
Электронная формула дубния: [Rn] 5f14 6d3 7s2.
- Валентные электроны: 5 (6d3 7s2).
- Механизм: Потеря всех 5 электронов дает стабильную конфигурацию остова [Rn] 5f14.
По химическому соединению (Алгебраический расчет)
Пример для DbCl5:
- 1. Хлор — -1.
- 2. 5 атомов хлора дают заряд -5.
- 3. x + (-5) = 0, значит x = +5.
Примеры степеней окисления дубния
| СО | Характеристика | Примеры |
|---|---|---|
| +5 | Наиболее стабильная. | DbCl5 |
Шпаргалка
- +5 — главная степень окисления.
- Аналог тантала — проявляет свойства группы 5.
Дубний вне учебника: что скрывает наука?
Релятивистские эффекты:
Из-за высокой скорости электронов орбитали дубния искажаются. Это приводит к тому, что стабильность связи Db-Cl отличается от Nb-Cl и Ta-Cl.
Химические комплексы:
Дубний в кислых растворах образует комплексы [DbOCl4]—, что подчеркивает его отличия от более легких аналогов.
Сложности синтеза:
Дубний существует лишь миллисекунды, и исследование его химии — это вершина достижений современной радиохимии.
Интересный факт: Первые эксперименты по изучению химии дубния проводились на атомах, время жизни которых составляло менее 1 секунды, что является мировым рекордом для химических исследований.
Пример решения задачи:
▶️ Дано:
Соединение: DbCl5 (хлорид дубния V).
⌕ Найти:
Определите степень окисления (СО) дубния.
✨ Решение:
Суммарный заряд 5 хлоров: 5 * (-1) = -5.
x + (-5) = 0 ⇒ x = +5.
✅ Ответ:
СО дубния в DbCl5 равна +5.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: дубний получен искусственно.
Часто задаваемые вопросы
Главной и наиболее устойчивой степенью окисления является +5.
Это обусловлено выраженной металлической природой элемента и его низкой электроотрицательностью, что делает невозможным присоединение электронов.
Из-за положения в таблице: Дубний относится к 5-й группе, для которой состояние +5 является максимально устойчивым энергетическим пределом.
Из-за релятивистских эффектов: Околосветовые скорости электронов делают состояние +5 энергетически безальтернативным.
Сложность эксперимента: Сверхкороткое время жизни элемента позволяет зафиксировать только самое устойчивое состояние.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.