Теория:
Степень окисления гелия (He) во всех стабильных химических условиях принимает единственное значение — 0.
Являясь первым представителем благородных газов, гелий обладает самой устойчивой электронной оболочкой (1s2) среди всех элементов.
Отрицательные степени окисления для него физически невозможны, так как у атома нет свободных орбиталей на первом энергетическом уровне для принятия дополнительных электронов.
Например для основной СО 0: гелий существует в виде одноатомного газа He.
Его электронная оболочка полностью завершена (дублет), что делает его абсолютно инертным в обычных условиях.
Энергия ионизации гелия — самая высокая в Периодической системе.
Это означает, что ни один химический окислитель не способен «оторвать» у него электроны, чтобы придать ему положительную степень окисления.
Для сравнения, теоретические СО: в условиях экстремально высокого давления ученым удалось синтезировать структуру Na2He.
Но даже в таких условиях гелий не образует полноценных химических связей, фактически оставаясь в степени окисления 0.
- Почему только 0? Электронная формула 1s2 соответствует полностью заполненному уровню. В отличие от тяжелых газов (ксенона), у гелия нет d-орбиталей для «распаривания» электронов.
- Почему нет положительных СО? Электроны первого уровня находятся максимально близко к ядру и удерживаются с огромной силой, которую невозможно преодолеть в ходе химической реакции.
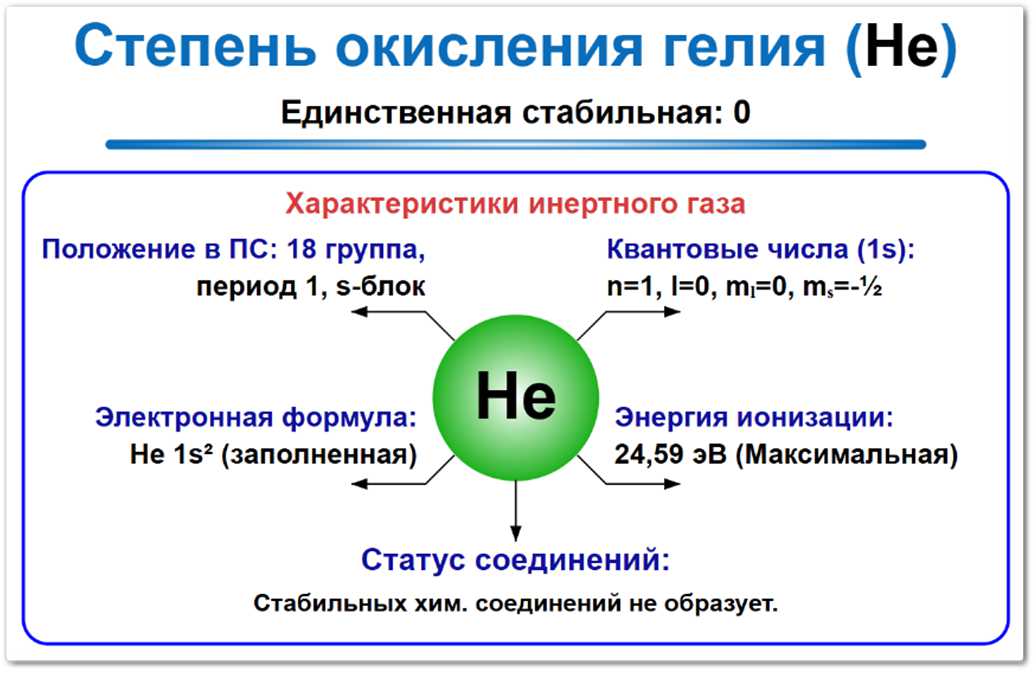
Рис. 1. Гелий в состоянии 0. Минимальный атомный радиус обеспечивает максимальное притяжение электронов к ядру.
Содержание страницы
- 1. Почему у гелия стабильная степень окисления?
- 2. Степень окисления гелия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 3. 4 способа определить степень окисления гелия
- 3.1. По таблице Менделеева
- 3.2. По валентности (Число связей)
- 3.3. По электронной конфигурации
- 3.4. По химическому соединению (Алгебраический расчет)
- 4. Примеры степеней окисления гелия
- 5. Шпаргалка для гелия
- 6. Пример решения задачи:
- 7. Проверка знаний
- 8. Часто задаваемые вопросы
Почему у гелия стабильная степень окисления?
Стабильность СО 0 обусловлена завершенностью его единственного электронного слоя, который находится в «энергетической яме».
- В простом веществе (He0): Заряд равен 0. Конфигурация:
1s [↑↓]. - В ионизированном состоянии (He+): Встречается в космосе (звездная плазма), но не образует стабильных химических веществ.

Рис. 2. Электронная конфигурация и квантовые ячейки гелия (He). Стабильная 1s2 оболочка обуславливает химическую инертность и степень окисления 0.
Степень окисления гелия в соединениях
Поскольку гелий практически не вступает в реакции, его степень окисления остается неизменной:
- Гелий газообразный (He): He 0.
- Гелат натрия (Na2He): He 0.
- Ван-дер-ваальсовы комплексы: He 0.
Высшая степень окисления
Высшая степень окисления гелия в химии равна 0. Альфа-частицы (He2+) существуют как физические объекты, но не как часть молекул.
Низшая степень окисления
Для гелия низшая степень окисления равна 0.
Важно: Гелий — самый химически инертный элемент. Если ксенон можно «заставить» реагировать с фтором, то для гелия таких реагентов не существует.
4 способа определить степень окисления гелия
По таблице Менделеева
- Семейство: Благородные газы (s-элемент).
- Валентные электроны: 2.
- Атомная масса: 4,0026 а.е.м.
По валентности (Число связей)
В отличие от других элементов, валентность гелия в стабильных условиях равна 0.
- В свободном состоянии: Атом гелия не образует химических связей. Его валентность — 0.
- В экстремальных условиях: Даже в соединениях под давлением связи носят нековалентный характер, поэтому классическая валентность остается равной нулю.
По электронной конфигурации
- Электронная формула гелия: 1s2.
- Атому гелия степени окисления выше нуля недоступны из-за отсутствия пустых орбиталей на валентном слое.
По химическому соединению (Алгебраический расчет)
Пример для простого вещества (He):
Согласно правилам, степень окисления элемента в одноатомном простом веществе всегда равна 0.
Сумма СО атомов в молекуле равна 0. Так как атом один: x = 0.
Примеры степеней окисления гелия
| СО | Характеристика | Где встречается |
|---|---|---|
| 0 | Постоянная. Единственно возможная в химии. | Воздух, недра звезд, баллоны. |
Шпаргалка для гелия
- 0 — единственная и абсолютно стабильная форма существования в любых химических условиях.
- Инертность — не вступает в реакции с окислителями (даже с фтором) из-за рекордно высокой энергии ионизации.
- s-элемент — свойства определяются полностью завершенным и компактным 1s2-подуровнем.
Пример решения задачи:
▶️ Дано:
Вещество: Жидкий гелий (используется для охлаждения МРТ).
⌕ Найти:
Определите СО гелия в этом состоянии.
✨ Решение:
Переход из газообразного состояния в жидкое — это физический процесс. Химические связи не образуются, состав атома не меняется. Степень окисления простого вещества всегда равна нулю.
✅ Ответ:
He(0).
Проверка знаний
Показать ответы
Правильные ответы: 2, 4, 5.
Разбор ошибок:
1 — неверно: фтор (F) самый электроотрицательный, у гелия электроотрицательность формально не определена из-за отсутствия связей.
3 — неверно: HeO не существует.
Часто задаваемые вопросы
Нет, его оболочка 1s2 полностью заполнена, а для новых электронов нет места на первом уровне.
У ксенона большой радиус и есть d-орбитали для распаривания электронов. У гелия электроны прижаты к ядру «намертво».
В нормальных условиях — нет, его степень окисления всегда 0. Однако при колоссальном давлении (более 1 млн атмосфер) ученым удалось создать стабильное соединение гелид натрия (Na2He).
В таких «экстремальных» условиях гелий ведет себя не как газ, а как часть кристаллической решетки, хотя классических химических связей при этом не образует.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.