Теория:
Степень окисления бория (Bh) в химических соединениях проявляет высшую и наиболее характерную степень окисления +7.
Это обусловлено положением элемента в 7-й группе Периодической системы, где он является тяжелым аналогом марганца (Mn), технеция (Tc) и рения (Re).
Кроме того, выделяют показатель 0, который относится к борию в виде простого вещества (радиоактивный переходный металл).
Например для наиболее стабильной СО +7: в соединении BhO3Cl (триоксихлорид бория) заряд иона равен +7. В этом состоянии борий ведет себя как типичный гомолог рения.
Для сравнения, другие СО: теоретически для бория возможны степени окисления +5, +4 и +3, однако в экспериментах по химии «одного атома» наиболее устойчивым и подтвержденным является именно семивалентное состояние.
- Почему +7? Электронная формула бория [Rn] 5f14 6d5 7s2 предполагает участие всех семи валентных электронов в образовании связей, что соответствует высшей валентности группы.
- Почему другие СО менее вероятны? Для тяжелых d-элементов 7-й группы высшая степень окисления энергетически выгодна при взаимодействии с сильными окислителями (кислородом), формируя устойчивые оксигалогениды.
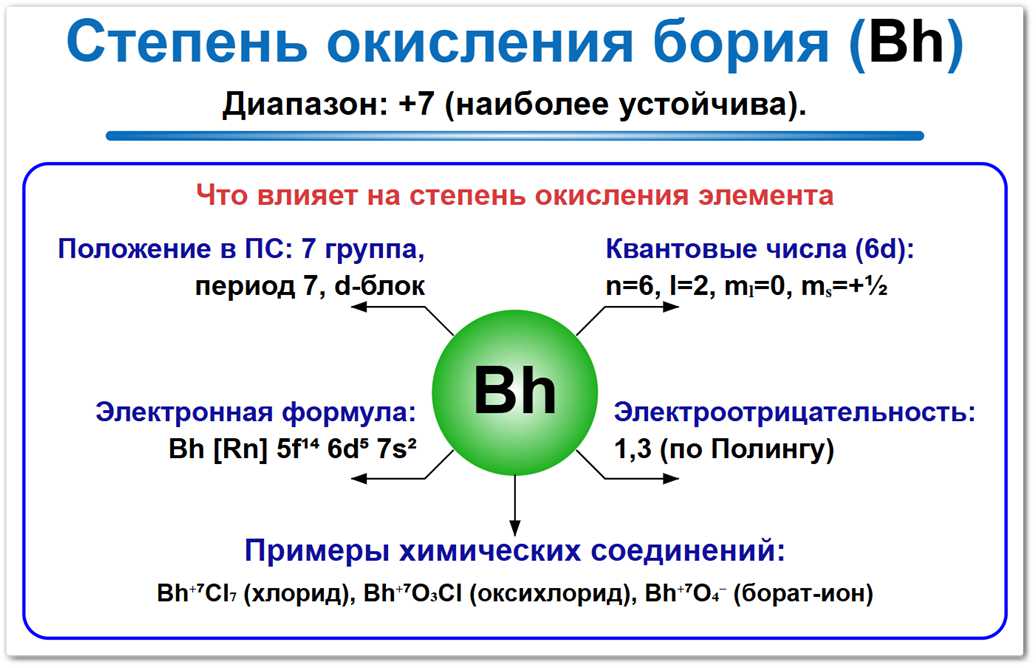
Рис. 1. Основная степень окисления бория: 0 и +7.
Состояние +7 является единственным надежно зафиксированным в ходе термохроматографических экспериментов с летучими соединениями бория.
Важно заметить, что борий — чрезвычайно короткоживущий элемент. Самые стабильные изотопы имеют период полураспада в несколько секунд.
Его изучение требует сложнейших экспресс-методов химической идентификации буквально по нескольким атомам.
На свойства бория влияют релятивистские эффекты, которые стабилизируют 7s-орбитали, что может слегка отличать его химическую активность от рения.
Содержание страницы
- 1. Почему +7 — самая устойчивая степень окисления у бория
- 2. Степень окисления бория в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему борий предпочитает заряд +7?
- 4. 4 способа определить степень окисления бория
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления бория
- 6. Шпаргалка
- 7. Борий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +7 — самая устойчивая степень окисления у бория
Стабильность определяется максимальным использованием валентных электронов 6d и 7s подоболочек.
- В простом веществе (Bh0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d5 7s2. - В семивалентном ионе (Bh+7): Борий формально отдает 7 электронов. Конфигурация:
[Rn] 5f14(устойчивый инертный остов).

Рис. 2. Схема образования степени окисления +7: вовлечение 6d и 7s электронов.
Степень окисления бория в соединениях
- Триоксихлорид бория (BhO3Cl): Bh +7.
- Триоксибромид бория (BhO3Br): Bh +7.
- Перборат-ион (BhO4—): Bh +7.
Высшая степень окисления
Высшая степень окисления Bh равна +7.
Низшая степень окисления
Характерна степень окисления 0 для металлического состояния.
Промежуточные степени окисления
Хотя для марганца характерны +2, +4 и +6, для бория (как и для рения) они менее стабильны в аэробных условиях эксперимента.
Важно: Борий назван в честь датского физика Нильса Бора, создателя квантовой модели атома.
Почему борий предпочитает заряд +7?
- Групповая преемственность: В 7-й группе стабильность высшей СО растет сверху вниз (от Mn к Re и далее к Bh).
- Энергетика связей: Образование соединений с кислородом (оксигалогенидов) позволяет борию достичь наиболее энергетически выгодного состояния.
4 способа определить степень окисления бория
По таблице Менделеева
- Семейство: Трансактиноиды (d-элементы).
- Валентные электроны: 7.
- Атомная масса: ~270 а.е.м.
По валентности (Число связей)
Валентность бория (Bh) в ключевых соединениях стабильно равна VII.
Как аналог рения, он формирует устойчивые молекулы, где атом бория связан с тремя атомами кислорода и одним галогеном.
Детальные примеры:
- В BhO3Cl: Центральный атом Bh образует три двойные связи с кислородом и одну одинарную с хлором.
- В потенциальных оксидах (Bh2O7): Аналогично Re2O7, борий проявляет свою высшую валентность через объединение с кислородными мостиками.
По электронной конфигурации
Электронная формула бория: [Rn] 5f14 6d5 7s2.
Как происходит ионизация:
- Валентные электроны: У бория 7 электронов на валентных орбиталях (пять 6d и два 7s).
- Механизм: При взаимодействии с сильными электроотрицательными элементами все 7 электронов вовлекаются в общие пары.
- Итог: Достигается электронная конфигурация [Rn]5f14, что характерно для ионов в высшей СО для d-металлов начала и середины периодов.
По химическому соединению (Алгебраический расчет)
Пример для BhO3Cl:
- 1. Кислород (O) имеет СО -2. Суммарно для трех атомов: 3 · (-2) = -6.
- 2. Хлор (Cl) имеет СО -1.
- 3. Общий отрицательный заряд: (-6) + (-1) = -7.
- 4. Обозначим СО бория за x. Уравнение электронейтральности: x + (-7) = 0.
- 5. Решение: x = +7.
✅ Вывод: Степень окисления бория в триоксихлориде равна +7.
Примеры степеней окисления бория
| СО | Характеристика | Примеры |
|---|---|---|
| +7 | Наиболее стабильная высшая СО. | BhO3Cl |
Шпаргалка
- +7 — главная степень окисления.
- Химический двойник рения — при изучении бория ученые всегда сравнивают его результаты с поведением Re.
Борий вне учебника: что скрывает наука?
Эксперименты в Дубне и Дармштадте:
Химия бория была доказана экспериментально путем синтеза летучего оксихлорида.
Ученым пришлось разработать систему, которая за доли секунды переводит отдельные атомы бория из мишени ускорителя в газовую фазу и реагирует с хлором и кислородом.
Релятивистская стабилизация:
У бория 7s-электроны «крепче» держатся за ядро из-за релятивистских эффектов.
Это могло бы сделать переход в состояние +7 сложнее, чем у рения, но на практике борий все же достигает этой СО, подтверждая свою принадлежность к группе.
Поиски в природе:
Как и все трансактиноиды, борий отсутствует в земной коре. Все данные о нем получены искусственным путем, что делает его «чисто кабинетным» элементом, оживающим лишь на кончике детектора на несколько мгновений.
Интересный факт: Первоначально группа из ГСИ (Дармштадт) предложила название «Нильсборий» с символом Ns. Однако IUPAC решил упростить его до «Борий», так как фамилии ученых в названиях элементов обычно используются без имен.
Пример решения задачи:
▶️ Дано:
Соединение: BhO3Br (триоксибромид бория).
⌕ Найти:
Определите степень окисления (СО) бория.
✨ Решение:
1. Кислород (O) имеет СО -2. Три атома дают: 3 · (-2) = -6.
2. Бром (Br) как галоген в данном соединении имеет СО -1.
3. Сумма отрицательных зарядов: (-6) + (-1) = -7.
4. Сумма СО всех атомов в нейтральной молекуле равна 0. Обозначим СО бория за x:
x — 7 = 0 ⇒ x = +7.
✅ Ответ:
СО бория (Bh) в данном соединении равна +7.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: высшая СО бория +7, а не +5.
Часто задаваемые вопросы
Самая важная и экспериментально подтвержденная — +7. Это «визитная карточка» элементов 7-й группы.
У тяжелых элементов (4d, 5d и 6d серий) проявляется тенденция к стабилизации высших степеней окисления. Низкие СО (+2, +3), характерные для марганца, у бория крайне нестабильны.
Отсутствие отрицательных степеней окисления у (Bh) объясняется его физико-химической природой тяжелого металла 7-й группы:
Металлический характер: Как аналог рения, борий обладает низкой электроотрицательностью, поэтому ему энергетически выгодно отдавать электроны, а не притягивать их.
Электронная конфигурация: Его внешняя оболочка [Rn] 5f14 6d5 7s2 предрасположена к потере до 7 электронов для достижения стабильности (+7), а не к захвату новых для создания отрицательного заряда.
Релятивистские эффекты: У сверхтяжелых элементов s-орбитали сильнее притянуты к ядро, что затрудняет присоединение лишних электронов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.