Теория:
Степень окисления бария в подавляющем большинстве соединений принимает значение +2, в свободном состоянии она равна 0.
В отличие от переходных металлов, барий является типичным представителем щелочноземельных металлов, поэтому проявление других состояний для него нехарактерно.
Например для высшей СО +2: в соединении BaO (оксид бария) степень окисления металла равна +2.
Это происходит потому, что барий находится во 2-й группе и при взаимодействии с таким сильным окислителем, как кислород.
Он полностью задействует свои 2 валентных электрона (6s2), достигая максимально возможного заряда и устойчивой оболочки инертного газа ксенона.
Для сравнения, отрицательная СО: для бария химически невозможна в обычных условиях.
Здесь ситуация однозначна: барий обладает очень низкой электроотрицательностью (0,89) и является мощным восстановителем. Он всегда стремится отдать электроны, а не принимать их на свои орбитали.
Такие состояния, как -1 или -2, не зафиксированы даже в сложных комплексах, так как металл мгновенно переходит к положительному заряду, который для него энергетически естественнее.
Промежуточные же степени окисления, такие как +1, являются крайне «неудобными» для атома.
Обладая конфигурацией [Xe] 6s2, барию проще сразу отдать пару электронов, чтобы достичь стабильной формы +2.
Соединения бария(I) могут существовать лишь мгновения в газовой фазе при сверхвысоких температурах.
Именно поэтому барий не склонен к диспропорционированию — его химия стабильна и предсказуема в рамках одного основного состояния.
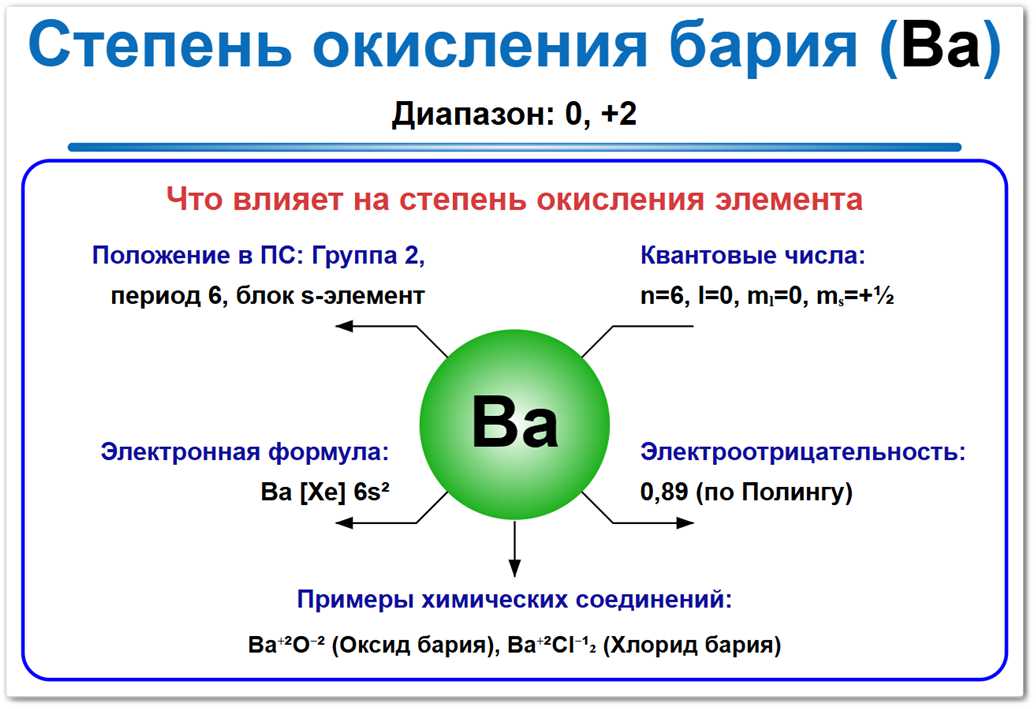
Рис. 1. Возможные степени окисления бария: от 0 до +2. Наиболее устойчивая и единственно значимая форма — +2 (сульфаты, карбонаты), характерная для всех его минералов.
Обратите внимание, что химия бария во многом схожа с химией радия (Ra), своего соседа по группе, что проявляется в образовании крайне труднорастворимых сульфатов состава MeSO4.
На их формирование влияют электронное строение (6s2), положение во 2-й группе и низкое значение электроотрицательности 0,89 по шкале Полинга.
Содержание страницы
- 1. Почему у бария стабильная степень окисления?
- 2. Степень окисления бария в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления бария
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления бария
- 6. Шпаргалка для бария
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у бария стабильная степень окисления?
Причина стабильности высшего состояния бария заключается в возможности задействовать оба электрона 6s-орбитали, что при полном окислении приводит к достижению электронной конфигурации инертного газа ксенона.
- В простом веществе (Ba⁰): Заряд равен 0. Конфигурация:
6s [↑↓]. - В ионе (Ba+2): Барий отдает оба валентных электрона. Конфигурация:
[Xe].

Рис. 2. Процесс окисления бария: от активного щелочноземельного металла до стабильного катиона +2.
Степень окисления бария в соединениях
В зависимости от реагентов, барий в соединениях проявляет степень окисления, которая определяет высокую реакционную способность вещества:
- Хлорид бария (BaCl2): Ba +2, Cl -1.
- Сульфат бария (BaSO4): Ba +2, S +6, O -2.
- Пероксид бария (BaO2): Ba +2, O -1.
- Нитрат бария (Ba(NO3)2): Ba +2.
- Гидроксид бария (Ba(OH)2): Ba +2.
Высшая степень окисления
Высшая степень окисления бария равна +2. Это значение полностью соответствует номеру группы (II) в периодической системе и является пределом для данного элемента.
Низшая степень окисления
Отрицательные состояния для него невозможны, поэтому степень окисления бария равна 0 в металлическом виде — это наиболее типичное низшее состояние для этого элемента.
Промежуточные степени окисления
Степень окисления бария в веществах практически никогда не принимает значения +1.
Любые попытки синтезировать такие соединения приводят к их мгновенному окислению до стабильной формы +2.
Важно: Состояние +2 в виде сульфата (BaSO4) — это наиболее известная форма бария, используемая в медицине (рентгеноскопия), где степень окисления бария формула соединения всегда остается неизменной.
Почему степень окисления чаще положительная?
Знак заряда определяется ярко выраженной металлической природой элемента:
- Положительная СО (+): Барий очень легко отдает электроны любым неметаллам, достигая завершенного энергетического уровня.
- Нулевая СО (0): Характерна для чистого металла, который хранится под слоем керосина из-за высокой активности.
- Отрицательная СО (-): Физически невозможна из-за крайне низкого сродства к электрону.
Как определить степень окисления бария
По таблице Менделеева
- Семейство: s-элемент (щелочноземельный металл).
- Валентные электроны: 2 (на 6s-подуровне).
- Атомная масса бария: 137 а.е.м.
По валентности (Число связей)
В отличие от d-элементов, валентность бария постоянна и всегда равна II.
- В оксиде (BaO): Атом бария образует две связи с кислородом. Его валентность — II, а степень окисления равна +2.
- В пероксиде (BaO2): Барий также связан двумя связями с пероксидной группой. Валентность — II, СО бария — +2.
По электронной конфигурации
- Электронная формула бария: [Xe] 6s2.
- Атому бария степени окисления +2 достичь максимально выгодно, так как это полностью освобождает внешний слой и делает ион очень стабильным.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Ba(NO3)2 (нитрат бария):
Сумма СО равна 0. Кислород -2, Азот +5. Обозначим Ba как x.
x + 2 · (+5) + 6 · (-2) = 0
x + 10 — 12 = 0 ⇒ x = +2
Примеры степеней окисления бария
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +2 | Высшая и единственно стабильная. Характерна для всех солей. | BaSO4, BaCl2, BaO |
| 0 | Металл. Активное состояние простого вещества. | Ba (слиток под маслом) |
Шпаргалка для бария
- +2 — единственная степень в химии, барий никогда не меняет её в реакциях.
- Яд — почти все растворимые соединения бария в СО +2 крайне токсичны.
- Цвет — ионы бария +2 окрашивают пламя в характерный желто-зеленый цвет.
Пример решения задачи:
▶️ Дано:
Соединение: BaO2 (пероксид бария).
⌕ Найти:
Определите СО бария.
✨ Решение:
В пероксидах группа O2 имеет общий заряд -2 (каждый O по -1). Уравнение: x + 2 · (-1) = 0 → x — 2 = 0 → x = +2.
✅ Ответ:
Ba(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: у бария только 2 валентных электрона, СО +4 невозможна.
5 — неверно: барий — активный металл, отрицательных СО не имеет.
Часто задаваемые вопросы
Единственно стабильной в соединениях является степень окисления +2.
В химии растворов и твердых тел — нет. Такие формы крайне неустойчивы и существуют только в виде короткоживущих частиц в плазме или газах.
Нет отрицательных степеней окисления по двум причинам:
Низкая электроотрицательность: Барий — типичный активный металл. Он крайне неохотно удерживает свои электроны и тем более не может притягивать чужие.
Энергетическая выгода: Барию гораздо проще отдать 2 электрона с внешнего уровня (6s2), чтобы получить стабильную оболочку инертного газа (ксенона), чем пытаться забрать 6 недостающих электронов для завершения октета.
