Теория:
Степень окисления неодима (Nd) в большинстве соединений принимает значение +3, значительно реже встречаются состояния 0, +2, +4.
Также существуют крайне нестабильные состояния (+5), которые проявляются только в специфических условиях (например, в матрицах инертных газов или сложных металлоорганических структурах).
Например для наиболее характерной СО +3: в соединении Nd2O3 (оксид неодима) степень окисления металла равна +3.
Это происходит потому, что неодим относится к семейству лантаноидов и при химическом взаимодействии он наиболее охотно отдает три электрона (два с 6s-подуровня и один с 4f-подуровня), достигая энергетически выгодного состояния.
Для сравнения, редкая СО +2: встречается в таких соединениях, как NdI2 (иодид неодима II).
Здесь ситуация иная: неодим отдает только два электрона, сохраняя избыточную электронную плотность на f-орбиталях. Такие состояния являются сильными восстановителями.
Такие состояния крайне нестабильны в присутствии воды или кислорода, так как металл стремится вернуться к положительному заряду +3, который для него энергетически естественнее в большинстве сред.
Промежуточные же или высшие степени окисления, такие как +4, являются «неудобными» для атома неодима и встречаются крайне редко.
Обладая конфигурацией [Xe] 4f4 6s2, неодиму проще всего остановиться на стабильной форме +3.
Именно поэтому соединения неодима в нетипичных степенях окисления часто проявляют высокую реакционную способность — они самопроизвольно стремятся перейти к устойчивому состоянию +3.
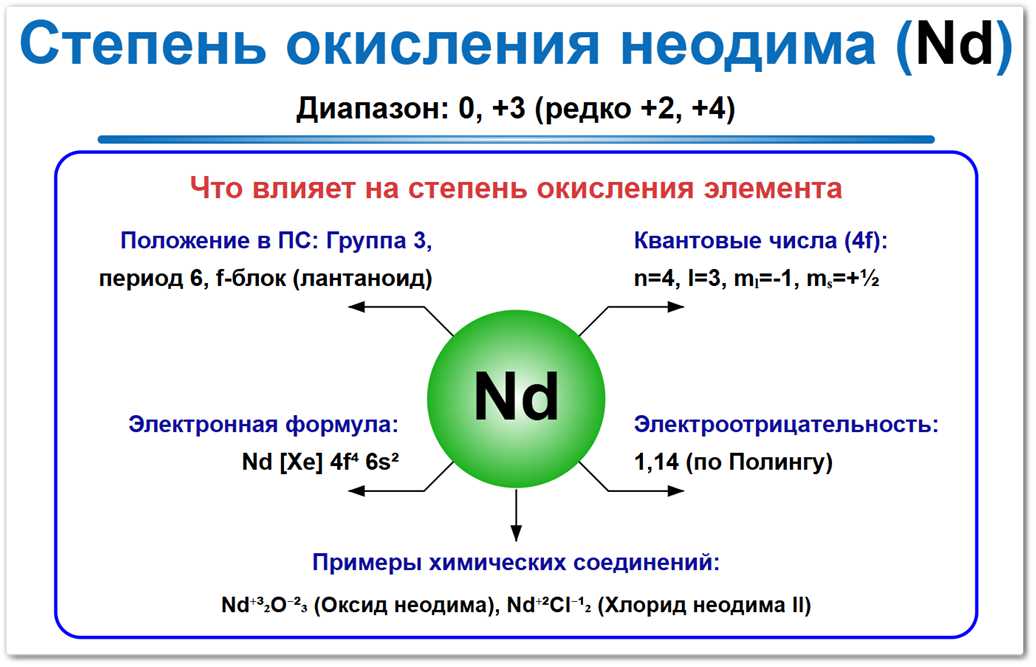
Рис. 1. Возможные степени окисления неодима: доминирующая форма — +3 (типичная для лантаноидов), а также редкие состояния +2 и +4.
Обратите внимание, что химия неодима во многом схожа с химией празеодима (Pr), своего соседа по ряду лантаноидов, однако способность неодима проявлять СО +4 выражена значительно слабее.
На их формирование влияют электронное строение (4f4 6s2), положение в семействе лантаноидов и значение электроотрицательности 1,14 по шкале Полинга.
Содержание страницы
- 1. Почему у неодима стабильная степень окисления?
- 2. Степень окисления неодима в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления неодима
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления неодима
- 6. Шпаргалка для неодима
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у неодима стабильная степень окисления?
Причина стабильности основного состояния неодима (+3) заключается в оптимальном балансе энергии ионизации и энергии кристаллической решетки (или гидратации), что делает потерю трех электронов наиболее выгодной.
- В простом веществе (Nd⁰): Заряд равен 0. Конфигурация:
6s2 4f4. - В ионе (Nd+3): Неодим отдает 3 электрона. Конфигурация:
[Xe] 4f3.

Рис. 2. Процесс окисления неодима: от металлического состояния до наиболее устойчивого состояния +3.
Степень окисления неодима в соединениях
В зависимости от реагентов, неодим в соединениях проявляет степень окисления, которая определяет физико-химические свойства вещества:
- Оксид неодима(III) (Nd2O3): Nd +3, O -2.
- Хлорид неодима(III) (NdCl3): Nd +3, Cl -1.
- Иодид неодима(II) (NdI2): Nd +2.
- Фторид неодима(IV) (NdF4): Nd +4 (крайне нестабилен).
- Металлический неодим (Nd): Nd 0.
Высшая степень окисления
Высшая степень окисления неодима может достигать +4, но она проявляется только в исключительных случаях (например, в комплексных фторидах). В обычной химии высшей устойчивой степенью считается +3.
Низшая степень окисления
Для неодима возможна степень окисления +2 в некоторых галогенидах, однако степень окисления неодима равна 0 в металлическом виде — это стандартное низшее состояние.
Промежуточные степени окисления
Степень окисления неодима в веществах почти всегда равна +3. Состояния +2 и +4 являются переходными или синтетически сложными и легко переходят в +3.
Важно: Состояние +3 — это «фундамент» химии неодима. Именно в этой степени окисления неодима формула соединения (например, Nd2Fe14B) обеспечивает уникальные магнитные свойства сверхмощных магнитов.
Почему степень окисления чаще положительная?
Знак заряда определяется металлической природой лантаноида:
- Положительная СО (+): Неодим легко отдает электроны неметаллам из-за низкой электроотрицательности.
- Нулевая СО (0): Характерна для чистого серебристо-белого металла.
- Отрицательная СО (-): Для лантаноидов в обычных химических системах нехарактерна.
Как определить степень окисления неодима
По таблице Менделеева
- Семейство: f-элемент.
- Валентные электроны: электроны 6s и 4f подуровней.
- Атомная масса неодима: 144,24 а.е.м.
По валентности (Число связей)
Как и у большинства редкоземельных элементов, валентность неодима обычно постоянна и равна III.
- В оксиде (Nd2O3): Атом неодима образует три связи с кислородом. Его валентность — III, а степень окисления равна +3.
- В хлориде (NdCl3): Неодим образует три связи с хлором. Валентность — III, СО неодима — +3.
По электронной конфигурации
- Электронная формула неодима: [Xe] 4f4 6s2.
- Атому неодима степени окисления +3 достичь легче всего, так как это связано с удалением двух 6s-электронов и одного 4f-электрона.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для Nd2(SO4)3 (сульфат неодима):
Сумма СО равна 0. Группа SO4 имеет заряд -2. Обозначим Nd как x.
2 · x + 3 · (-2) = 0
2x — 6 = 0 ⇒ x = +3
Примеры степеней окисления неодима
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Высшая (редкая). Нестабильна в обычных условиях. | Cs3[NdF7], NdF4 |
| +3 | Наиболее стабильная. Основная форма существования. | Nd2O3, NdCl3, Nd2(SO4)3 |
| +2 | Низкая (редкая). Сильный восстановитель. | NdI2, NdCl2 |
| 0 | Металл. Чистое вещество. | Nd (металлический) |
Шпаргалка для неодима
- +3 — единственно стабильная степень в растворах и на воздухе.
- Магнетизм — ионы неодима в СО +3 обладают неспаренными электронами, что делает их основой мощнейших постоянных магнитов.
- Цвет — соли неодима(III) имеют характерную сиреневую или розовую окраску, меняющуюся при разном освещении.
Пример решения задачи:
▶️ Дано:
Соединение: NdCl3.
⌕ Найти:
Определите СО неодима.
✨ Решение:
Хлор (Cl) в соединениях с металлами обычно равен -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Nd(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: в отличие от рутения, высшая степень неодима не превышает +4, и та крайне редка.
Часто задаваемые вопросы
Наиболее стабильной и часто встречающейся в химии является степень окисления +3.
Как и у большинства металлов, нет отрицательных степеней окисления по двум коротким причинам:
1. Низкая электроотрицательность.
2. Энергетическая невыгодность.
Неодим в редкой степени окисления +4 может проявлять свойства окислителя, стремясь перейти в +3.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.