Теория:
Степень окисления московия (Mc) в химических соединениях, согласно теоретическим расчетам и его положению в таблице, проявляет наиболее характерные значения +1 и +3.
Это обусловлено положением элемента в 15-й группе (пниктогены) Периодической системы.
В отличие от более легких аналогов (азота, фосфора, висмута), на химию московия колоссальное влияние оказывают релятивистские эффекты.
Кроме того, выделяют показатель 0, который относится к московию в виде простого вещества (предположительно, тяжелый нелетучий металл).
Например для предполагаемой стабильной СО +1: в соединении McCl (хлорид московия I) заряд иона равен +1.
В этом состоянии московий проявляет свойства, схожие с таллием (Tl+) более ярко, чем с висмутом, из-за стабилизации 7s2-электронной пары.
Для сравнения, другие СО: высшая степень окисления +5, характерная для азота или фосфора, для московия считается крайне нестабильной или недостижимой из-за «эффекта инертной пары».
- Почему +1 и +3? Электронная формула московия [Rn] 5f14 6d10 7s2 7p3. Из-за релятивистского сжатия 7s- и 7p1/2-орбиталей, электроны с них уходят неохотно, делая низшие степени окисления предпочтительными.
- Почему СО +5 менее вероятна? Энергия, необходимая для распаривания и отдачи всех пяти валентных электронов, слишком велика, что делает московий(V) химически «невыгодным».
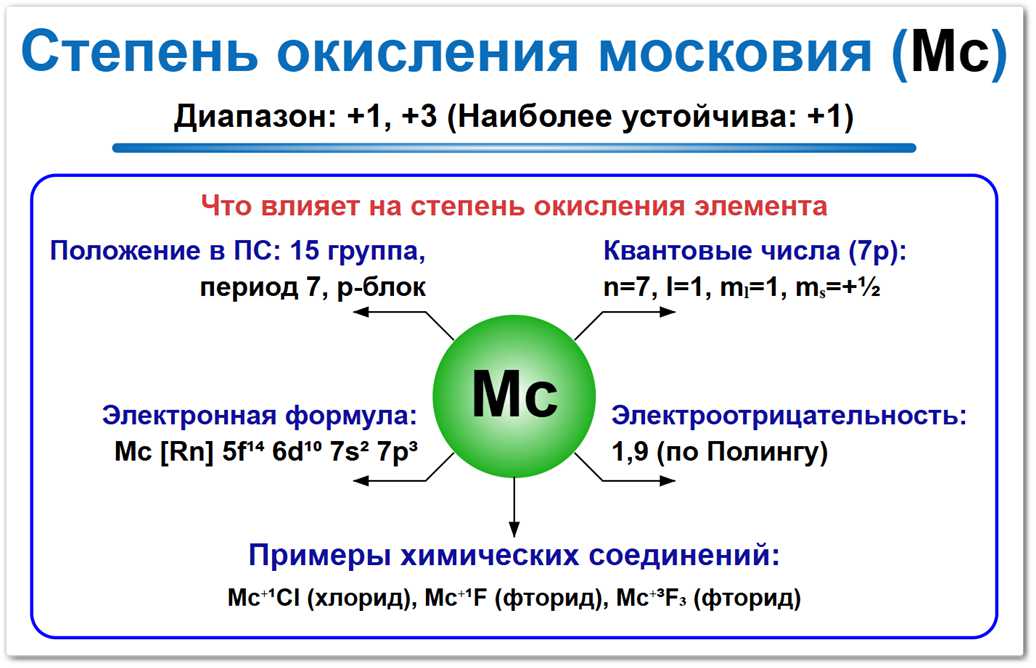
Рис. 1. Основные предполагаемые степени окисления московия: 0, +1 и +3.
Состояние +1 считается наиболее устойчивым в водных растворах (теоретически), в то время как +3 может проявляться в газофазных реакциях с сильными окислителями.
Важно заметить, что московий — сверхтяжелый элемент, впервые синтезированный в Дубне (Россия).
Его изотопы имеют крайне малые периоды полураспада (миллисекунды).
Из-за высокой радиоактивности и короткого времени жизни детальное изучение его химии «в пробирке» невозможно; ученые используют математическое моделирование и редкие эксперименты по «химии одного атома».
Содержание страницы
- 1. Почему +1 — наиболее вероятная степень окисления у московия
- 2. Степень окисления московия в соединениях (прогноз)
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему московий отличается от висмута?
- 4. 4 способа определить степень окисления московия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления московия
- 6. Шпаргалка
- 7. Московий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +1 — наиболее вероятная степень окисления у московия
Стабильность определяется релятивистским разделением p-подоболочки на уровни 7p1/2 и 7p3/2.
- В простом веществе (Mc0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d10 7s2 7p3. - В одно- и трехвалентном ионе: Московий теряет сначала один p-электрон (СО +1), затем оставшиеся два p-электрона (СО +3).

Рис. 2. Схема ионизации: стабилизация 7s-электронов приводит к преобладанию низких СО.
Степень окисления московия в соединениях (прогноз)
- Хлорид московия(I) (McCl): Mc +1.
- Фторид московия(III) (McF3): Mc +3.
- Гидрид московия (McH): Mc +1.
Высшая степень окисления
Высшая степень окисления Mc формально может достигать +5, но фактически ограничена +3.
Низшая степень окисления
Характерна степень окисления 0 в металлическом состоянии.
Промежуточные степени окисления
Степень окисления +3 рассматривается как промежуточная между стабильной +1 и нестабильной +5.
Важно: Московий назван в честь Московской области, где в Объединенном институте ядерных исследований (ОИЯИ) был открыт этот элемент.
Почему московий отличается от висмута?
- Релятивистские эффекты: Они делают ион Mc+ более стабильным, чем Bi+.
- Энергия ионизации: У московия она распределена так, что отрыв четвертого и пятого электронов требует колоссальных затрат энергии.
4 способа определить степень окисления московия
По таблице Менделеева
- Семейство: Постпереходные металлы (p-элементы).
- Валентные электроны: 5 (7s2 7p3).
- Атомная масса: [290] а.е.м.
По валентности (Число связей)
Валентность московия (Mc) теоретически варьируется от I до III.
Детальные примеры:
- В McCl: Московий образует одну ковалентную связь с хлором, проявляя валентность I.
- В McF3: С высокоэлектроотрицательным фтором московий может образовать три связи (валентность III).
По электронной конфигурации
Электронная формула московия: [Rn] 5f14 6d10 7s2 7p3.
- СО +1: Атом теряет один 7p-электрон. Конфигурация:
...7s2 7p2(с учетом спин-орбитального расщепления). - СО +3: Теряются все три 7p-электрона. Остается «инертная пара» 7s2.
По химическому соединению (Алгебраический расчет)
Пример для McCl3 (предполагаемый трихлорид):
- 1. Хлор (Cl) имеет СО -1.
- 2. 3 атома хлора: 3 · (-1) = -3.
- 3. Уравнение для московия (x): x + (-3) = 0.
- 4. Решение: x = +3.
Примеры степеней окисления московия
| СО | Характеристика | Примеры |
|---|---|---|
| +1 | Наиболее стабильная (прогноз). | McCl, McOH |
| +3 | Возможная в жестких условиях. | McF3 |
Шпаргалка
- +1 — ожидаемая основная СО.
- Эффект инертной пары — причина сходства с таллием больше, чем с висмутом.
Московий вне учебника: что скрывает наука?
Химия «вспышки»:
Поскольку московий живет доли секунды, химические опыты с ним проводятся методом «термохроматографии». Атомы газа-носителя проносят атом московия через золотую трубку, и по температуре его осаждения ученые понимают, насколько он химически активен.
Сходство с благородными газами?
Некоторые расчеты показывают, что из-за релятивистских эффектов московий может быть менее активным металлом, чем ожидается, проявляя почти «благородный» характер в СО 0.
Интересный факт: Открытие московия подтвердило существование «острова стабильности» — области сверхтяжелых ядер, которые живут дольше своих соседей.
Пример решения задачи:
▶️ Дано:
Соединение: McF3 (предполагаемый фторид московия III).
⌕ Найти:
Определите степень окисления (СО) московия.
✨ Решение:
Фтор — самый электроотрицательный элемент, его СО всегда -1.
Три атома фтора дают суммарный заряд: 3 · (-1) = -3.
Для нейтральности молекулы: x + (-3) = 0, отсюда x = +3.
✅ Ответ:
СО московия (Mc) в данном соединении равна +3. (Примечание: это состояние менее стабильно, чем +1).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: высшая СО +5 крайне нестабильна из-за эффекта инертной пары.
Часто задаваемые вопросы
Московий — очень тяжелый атом с выраженными металлическими свойствами. Его электроотрицательность слишком низка, чтобы притягивать электроны и образовывать стабильные отрицательные ионы.
Наиболее важной для понимания химии элемента считается +1.
Московий — типичный металл. Его электроотрицательность слишком мала, а внешние электроны удерживаются слишком слабо, чтобы он мог притягивать и удерживать дополнительные (чужие) электроны для создания отрицательного заряда.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.