Угольная кислота это слабая неорганическая кислота, сложное вещество, второе название углекислота (карбоновая кислота), химическая формула угольной кислоты H2CO3.
Основное применение угольной кислоты в пищевой промышленности в качестве добавки для газированных напитков.
Что такое угольная кислота и её соли
Двуокись углерода является ангидридом угольной кислоты. Угольная кислота H2CO3 сама по себе весьма непрочное вещество и существует только в водных растворах.
При выделении ее из растворов она легко распадается на воду и двуокись углерода :
H2CO2 ⇄ H2O + CO2
Угольная кислота является очень слабым электролитом , тем не менее , будучи двухосновной , она образует два ряда солей :
Средние — карбонаты.
Кислые — бикарбонаты.
Углекислоту можно определить как углеродсодержащее соединение, имеющее химическую формулу H2CO3.
Растворы углекислого газа в воде содержат небольшие количества этого соединения.
Химическая формула угольной кислоты также может быть записана как OC(OH)2, потому что в этом соединении имеется одна двойная связь углерод-кислород.
Углекислоту часто можно описать как респираторную кислоту по той причине, что это единственная кислота, выдыхаемая легкими человека в газообразном состоянии.
Она образует бикарбонат и карбонатные соли и это слабая кислота.
Угольная кислота H2CO3 способна растворять известняк, что приводит к образованию бикарбоната кальция (Ca(HCO3)2). Это основная причина различных особенностей известняка, включая сталактиты и сталагмиты.
Структурная формула угольной кислоты
Структура углекислоты или H2CO3 может быть проиллюстрирована ниже.
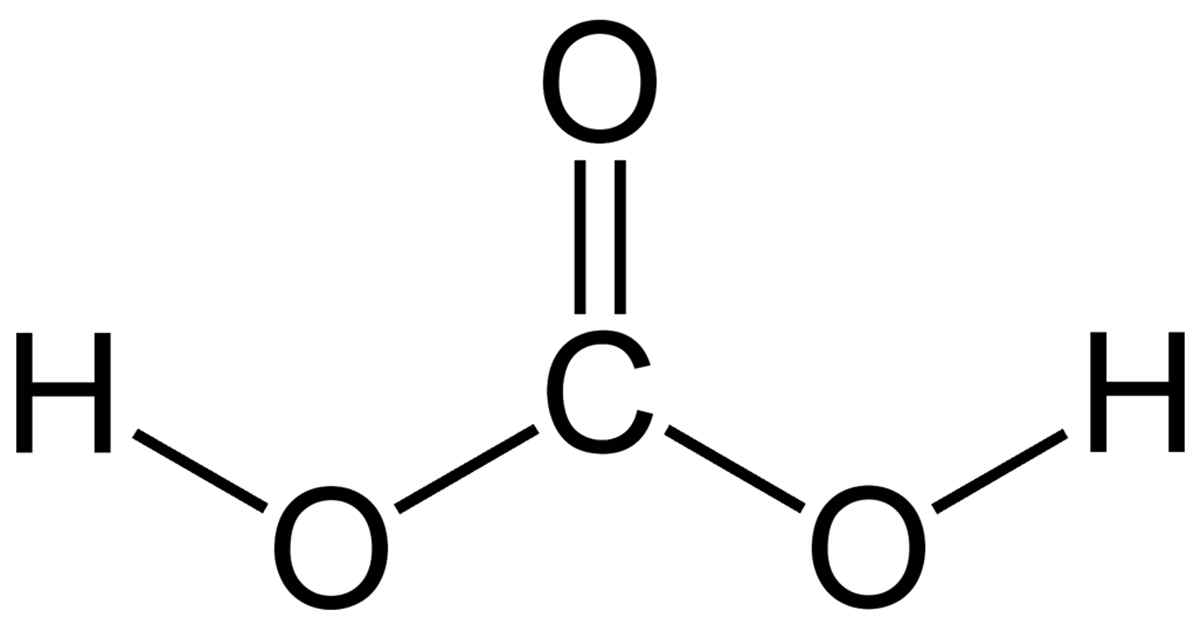
Структура углекислоты состоит из одной углерод-кислородной двойной связи и двух углерод-кислородных одинарных связей.
Атомы кислорода, которые участвуют в единственной связи с углеродом, каждый содержат по одному атому водорода, присоединенному к ним.
Получение
Углекислота, образующаяся в результате гидролиза и растворения CO2 в воде, является основным природным выщелачивающим агентом в различных экосистемах умеренного климата.
Угольная кислота нестабильна, слаба и быстро диссоциирует на бикарбонатные ионы (HCO3–) и ионы водорода (H+). Когда CO2 растворяется в воде, он участвует в химическом равновесии, как указано ниже.
CO2 + H2O ⇌ H2CO3
Однако при химическом равновесии, описанном выше, лишь небольшое количество диоксида углерода превращается в углекислоту.
Физические свойства
1. Молярную массу углекислоты можно определить как 62,024 грамма на моль.
2. Соединение H2CO3 имеет значение pKa, равное 3,6.
3. В стандартном состоянии он имеет плотность 1,668 грамма на кубический сантиметр.
4. Как правило, это соединение существует в виде раствора. Но сообщалось, что ученые НАСА подготовили твердые образцы H2CO3.
5. Сопряженным основанием, соответствующим углекислоте, является бикарбонат.
Химические свойства
1. H2CO3 нестабилен по своей природе, и это слабая кислота.
2. В присутствии воды он подвергается частичной диссоциации с образованием ионов HCO3– (бикарбонат) и H+.
3. Угольная кислота является дипротовой кислотой, и, следовательно, она может образовывать два типа солей:
карбонаты и бикарбонаты.
4. Добавление небольшого количества основания к H2CO3 приводит к образованию бикарбонатных солей, тогда как добавление основания в избыточных количествах приводит к образованию карбонатных солей.
5. Следует также отметить, что углекислота может быть получена при сжигании ископаемого топлива в промышленных масштабах или в качестве побочного продукта промышленных процессов ферментации.
Использование угольной кислоты (углекислоты)
Угольная кислота H2CO3 является важным соединением с широким спектром применения. Ниже перечислены некоторые виды применения углекислоты:
1. Приготовление игристого вина, газированной воды и других газированных напитков связано с использованием углекислоты.
2. H2CO3 может быть использован для осаждения различных солей аммония, таких как персульфат аммония.
3. Это помогает в выведении углекислого газа из организма.
4. H2CO3 протонирует многие основания, которые содержат азот в сыворотке крови.
5. Стригущий лишай и другие дерматиты лечат путем нанесения углекислоты на пораженный участок.
6. Растворы, содержащие это соединение, гораздо более эффективны при чистке контактных линз.
7. Его можно принимать внутрь, чтобы вызвать рвоту, когда это необходимо (например, в случае передозировки препарата).
Важность углекислоты в крови
Ион или молекула бикарбоната является промежуточным звеном для выведения двуокиси углерода из организма человека в процессе дыхательного газообмена.
Реакции гидратации, протекающие с участием двуокиси углерода, протекают очень медленно, особенно в отсутствие подходящего катализатора.
Присутствие семейства ферментов, называемых карбоангидразами, в красных кровяных тельцах приведет к увеличению скорости реакции.
Ферменты карбоангидразы катализируют превращение воды и углекислого газа в диссоциированные ионы углекислоты.
При этом образуются бикарбонатные анионы, которые растворяются в плазме крови.
Эта катализируемая реакция обратится вспять в легких, приводя к образованию CO2, а затем к выдыханию.
Кислотность углекислоты
Угольная кислота описывается как карбоновая кислота, которая содержит замещенную гидроксильную группу.
Ее также называют полипротонной кислотой. На самом деле это соединение является дипротонным и, следовательно, имеет два протона, которые диссоциируют от первичной исходной молекулы.
Таким образом, существуют две константы диссоциации, где первая относится к диссоциации на бикарбонат-ион.
Естественная кислотность дождевой воды
Чистая вода нейтральна по своей природе, то есть имеет рН 7. Но незагрязненная дождевая вода по своей природе слегка кислая, то есть имеет рН ниже 7.
Естественная кислотность дождевой воды составляет около 5,6, что делает ее кислой по своей природе.
Нужно помнить, что pH, проще говоря, — это не что иное, как мера концентрации ионов водорода в тестируемом растворе.
При тестировании природной, незагрязненной дождевой воды обнаруживается, что кислотная природа обусловлена тремя газами, присутствующими в воздухе.
Эти газы, называемые диоксидом углерода, оксидом азота и диоксидом серы, находятся в самом нижнем слое атмосферы Земли, называемом тропосферой.
Естественным источником углекислого газа в атмосфере является то, что углекислый газ образуется при разложении органических материалов на земле.
По сравнению с двумя другими газами, диоксид углерода вносит наибольший вклад в кислотную природу незагрязненной дождевой воды, поскольку он присутствует в самой высокой концентрации.
Концентрация диоксида углерода составляет 355 частей на миллион. Частей на миллион — вот что означает «промилле».
Соли угольной кислоты
Углекислые соли интересны тем , что при действии на них кислот выделяется двуокись углерода:
K2CO3 + 2HCl = 2KCl + H2CO3
При обработке двуокиси углерода и водой карбонаты превращаются в бикарбонаты.
При нагревании происходит обратное превращение :
CaCO3 + CO2 + H2O ⇄ Ca(HCO3)2
Карбонаты большей частью в воде не растворимы , за исключением карбонатов щелочных металлов и аммония.
Бикарбонаты растворимы лучше. Среди карбонатов особого внимания заслуживает карбонат кальция CaCO3, встречающийся в трёх видах :
Мрамор.
Известняк.
Мел.
Мрамор
Мрамор — твёрдое , кристаллическое вещество магматического происхождения. Он постепенно выкристаллизовался внутри остывающей магмы.
Часто мрамор бывает окрашен примесями в разные цвета. Мрамор легко полируется по этому широко используется как отделочный материал для облицовки строительных сооружений и в скульптуре.
Известняк
Известняк — осадочная порода органического происхождения , нередко в известняке можно обнаружить остатки древних животных , главным образом моллюсков в известковых раковинах.
Иногда они бывают довольно крупными , а иногда видны под микроскопом. За миллионы лет известняк уплотнился и стал настолько твёрдым , что его применяют иногда как строительный материал.
Но в настоящее время он как строительный материал вытесняется более дешевыми , лёгкими и удобными искусственными видами. Известняк используется в основном для получения извести.
Мел
Мел — Мягкая осадочная порода белого цвета. Применяется в строительстве , при изготовлении зубного порошка и паст.
Другие соли угольной кислоты
Исключительный интерес представляет сода Na2CO3 , встречающаяся иногда в природе , в так называемых содовых озёрах.
Но природная добыча соды практически вытеснена более дешевым искусственным получением этого продукта.
Если сода содержит кристаллизационную воду , то она называется кристаллической содой Na2CO3 · 10H2O , если же не содержит её , то кальцинированной содой.
Сода широко применяется в мыловарении , текстильной , бумажной и стиральных отраслях промышленности.
Двууглекислая сода или бикарбонат натрия или пищевая сода — NaHCO3 , применяется при выпечке кондитерских изделий как разрыхлитель теста.
А также в медицине при повышенной кислотности желудка, изжоге, диабете и т.д.
Карбонат калия K2CO3 или поташ как и сода применяется в мыловаренной промышленности и в производстве тугоплавкого стекла .
Статья на тему угольная кислота

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.