Автоклавное восстановление металлов из растворов водородом и другими газами
Восстановлению обязательно должно предшествовать образование водородного электрода, возможное при контакте газа с мелкими частицами металла, имеющим суммарно большую поверхность. Этим и объясняется необходимость затравки из ранее осажденного металла. Для реакции
Сu+ + Н2 = Сu + 2Н+;
В нейтральном растворе при рН2 = 101325 Па
С повышением кислотности и уменьшением рНз потенциал водородного электрода сдвигается в положительном направлении. Для осаждения наиболее благоприятны щелочные (аммиачные) растворы, в которых медь, никель, кобальт и некоторые другие металлы дают растворимые комплексы.
Для восстановления меди, никеля и кобальта аналогично» восстановлению водорода применяют окись углерода и сернистый газ, окислительно-восстановительные свойства которых можно характеризовать следующими системами:
СО + Н2O — 2е = СO2 + 2Н+; E0 = —0,1В,
SO2 + 2Н2O — 2е = SO24— + 4Н+; Е0 = 1,0 В.
Скорость цементации газами при обычных температурах и давлениях мала, а с превышением их значительно увеличивается. Как известно, водные растворы нельзя нагревать значительно выше 100° С: они закипают.
По этой причине восстановление проводят в толстостенных герметичных металлических сосудах— автоклавах, которые к тому же позволяют увеличить давление газа-восстановителя. С повышением давления температура кипения воды и водных растворов возрастает, для воды она достигает следующих величин, которые с малыми поправками свойственны и растворам:
р,кН/м2… 98,1 598,6 981 1580 1962
t°кип,°С .. 100 159,2 180,3 201,9 213,0
Статья на тему Автоклавное восстановление металлов из растворов водородом и другими газами

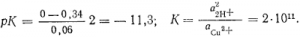
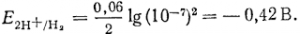
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.