Кремневый ангидрид или кремнезем, SiО2

Наиболее характерным и устойчивым соединением кремния является кремневый ангидрид, обычно называемый кремнеземом. Он встречается как в кристаллическом, так и аморфном виде.
Кристаллический кремнезем находится в природе главным образом в виде минерала кварца. Прозрачные, бесцветные кристаллы кварца, имеющие форму шестигранных призм с шестигранными пирамидами на концах, носят название горного хрусталя (рис. 113). Горный хрусталь, окрашенный примесями в лиловый цвет, называется аметистом, а в буроватый — дымчатым топазом. Но чаще кварц встречается в виде сплошных полупрозрачных масс, бесцветных или окрашенных в разные цвета. Одной из разновидностей кварца является кремень. К очень мелкокристаллическим разновидностям кварца относятся агат и яшма. Кварц входит также в состав многих сложных горных пород, например гранита, гнейса и др.
Из мелких зерен кварца состоит обыкновенный песок. Чистый песок — белого, цвета, но чаще он бывает окрашен соединениями железа в желтый или красноватый цвет.
Кристаллический кремнезем очень тверд, нерастворим в воде и плавится только в пламени гремучего газа или в электрической печи, превращаясь в бесцветную жидкость. При охлаждении этой жидкости получается прозрачная стекловидная масса аморфного кремнезема, по виду совершенно сходная с обыкновенным стеклом.
Аморфный кремнезем распространен в природе гораздо меньше, чем кристаллический. Из аморфного кремнезема построены панцыри некоторых низших водорослей. Скопления таких панцырей образуют местами довольно большие залежи и известны под названием трепела (диатомита), или инфузорной земли. Искусственным путем кремнезем получается в виде белого аморфного легкоподвижного порошка при прокаливании кремневой кислоты.
Резкое различие в физических свойствах кремнезема и угольного ангидрида объясняется тем, что последний состоит из отдельных молекул СО2, тогда как первый представляет собой полимер (SiO2)x. Структуру этого полимера, например структуру кварца, можно изобразить следующим образом:
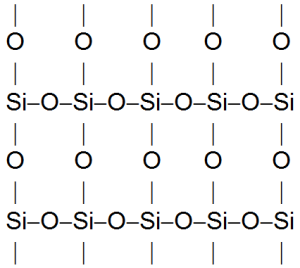
Каждый атом кремния находится в центре тетраэдра, по углам которого расположены атомы кислорода, каждый из которых, в свою очередь, связан с двумя атомами кремния. Чтобы разрушить кристалл кварца, надо разорвать большое число прочных связей кремния с кислородом. Этим обусловливается большая твердость кварца.
Кислоты, за исключением плавиковой, не действуют на кремнезем. Плавиковая же кислота, как уже было указано, легко вступает с ним в реакцию, образуя SiF4 и воду
SiO2 + 4HF = SiF4 + 2Н2O
Никакая другая кислота не действует подобным образом на окисел типичного металлоида.
Вы читаете, статья на тему Кремневый ангидрид, или кремнезем

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.