F фтор («флюор» Fluorum) химический элемент 17-й группы с порядковым номером 9 в периодической системе.
Находится во втором периоде. Имеет температуру плавления: -219.6 ℃, кипит при — 188,2°C. Плотность: 0.00158 г/см3.
Атомный радиус фтора составляет 147 мкм, что делает его самым маленьким атомом галогена.
Природный фтор — это изотоп 19F.
Активность молекул фтора гораздо выше, объясняется это сравнительно небольшой энергией диссоциации молекул фтора ( 158,34 кДж/моль ).
А также отсутствием у атома фтора d — орбиталей и следовательно дополнительных связей между атомами в молекуле.
Содержание страницы
Электронная формула
Электронная формула атома фтора:
1s2 2s2 2p5
Сокращенная электронная конфигурация F:
[He] 2s2 2p5
Электронно-графическая схема фтора (F)
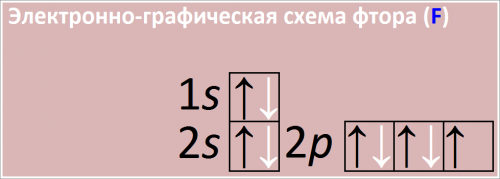
Рис. Схема распределения электронов по атомным орбиталям в атоме фтора.
Энергетические уровни
Распределение электронов по энергетическим уровням в атоме фтора F:
1-й уровень (K): 2
2-й уровень (L): 7

Рис. Распределение электронов по энергетическим уровням в атоме фтора F.
Валентные электроны фтора
Количество валентных электронов в атоме фтора — 7.
Таблица квантовых чисел фтора (N — главное, L — орбитальное, M — магнитное, S — спин).
| Орбиталь | N | L | M | S |
| s | 2 | 0 | 0 | +1/2 |
| s | 2 | 0 | 0 | -1/2 |
| p | 2 | 1 | -1 | +1/2 |
| p | 2 | 1 | 0 | +1/2 |
| p | 2 | 1 | 1 | +1/2 |
| p | 2 | 1 | -1 | -1/2 |
| p | 2 | 1 | 0 | -1/2 |
Степень окисления фтора равна: −1
Стабильные изотопы
| Изотоп | Протоны | Нейтроны | Атомная масса изотопа |
| 19F | 9 | 10 | ~18.99840322 |
Природный фтор состоит из одного 19F изотопа.
Известны изотопы фтора с массовыми числами от 14 до 31 (количество протонов 9, нейтронов от 5 до 22) и 2 ядерных изомера.
Изотоп 18F является источником позитронов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.