At астат (Astatium; от греч. — неустойчивый, астатин) — радиоактивный химический элемент 17-й группы, с порядковым номером 85 в периодической системе.
Атомный номер 85, атомная масса 210. Находится в шестом периоде. Температура плавления: 302 °C, температура кипения 302 °C. Плотность: 6.4 г/см3.
Содержание страницы
Электронная формула
Полная электронная формула атома астата в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p5
Сокращенная электронная конфигурация At:
[Xe] 4f14 5d10 6s2 6p5
Электронная формула атома астата в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 6s2 6p5
Электронно-графическая схема астата (At)
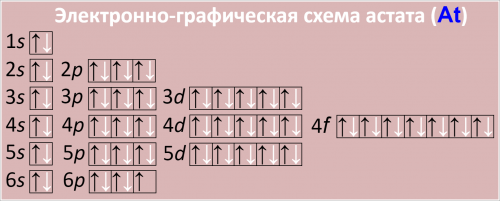
Рис. Схема распределения электронов по атомным орбиталям в атоме астата.
Энергетические уровни
Распределение электронов по орбиталям в атоме астата:
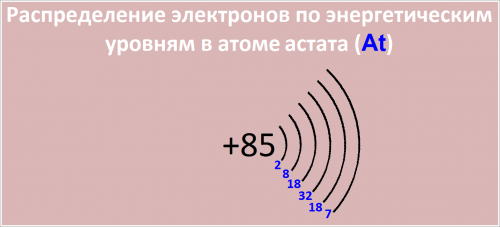
85 At )2 )8 )18 )32 )18 )7
Распределение электронов по энергетическим уровням в атоме At:
- -й уровень (K): 2
- -й уровень (L): 8
- -й уровень (M): 18
- -й уровень (N): 32
- -й уровень (O): 18
- -й уровень (P): 7
Рис. Распределение электронов по энергетическим уровням в атоме астата.
Валентные электроны астата
Количество валентных электронов в атоме — 7.
Таблица квантовых чисел At (N — главное, L — орбитальное, M — магнитное, S — спин).
| Орбиталь | N | L | M | S |
| s | 6 | 0 | 0 | +1/2 |
| s | 6 | 0 | 0 | -1/2 |
| p | 6 | 1 | -1 | +1/2 |
| p | 6 | 1 | 0 | +1/2 |
| p | 6 | 1 | 1 | +1/2 |
| p | 6 | 1 | -1 | -1/2 |
| p | 6 | 1 | 0 | -1/2 |
В соединениях астат проявляет степень окисления: -1, +1, +3, +5.
Стабильные изотопы
Стабильных изотопов у астата нет.
Известные изотопы (39) — альфа-радиоактивны, наиболее долгоживущий из них — 210At (период полураспада 8,3 ч).
Самые устойчивые от 207At до 211At.
Изотопы имеют короткий период полураспада — около 8,1 часа, а некоторые изотопы, нестабильны.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.