Теория:
Степень окисления тория (Th) в подавляющем большинстве стабильных химических соединений принимает значение +4.
Соединения +2 и +3 — лабораторная редкость, их получают искусственно и хранят в инертной атмосфере.
Этот элемент является типичным представителем семейства актиноидов.
Благодаря своей электронной конфигурации, торий стремится полностью освободить внешний и предвнешний уровни, достигая максимально устойчивого состояния.
Кроме того, существует показатель 0, который характерен для тория в виде простого вещества — тяжелого, тугоплавкого серебристо-белого металла.
Например для наиболее стабильной СО +4: в соединении ThO2 (диоксид тория) или ThCl4 (тетрахлорид тория) заряд иона равен +4. В этой форме торий проявляет максимальное химическое сходство с гафнием и цирконием.
Для сравнения, низшие СО (+2, +3): встречаются крайне редко, в основном в специфических безводных условиях или в составе необычных металлоорганических комплексов.
Примером может служить ThI2 (иодид тория II), однако такие вещества крайне нестабильны.
- Почему +4? Атому тория энергетически выгодно отдать все четыре валентных электрона (два с 6d-подуровня и два с 7s-подуровня), чтобы прийти к устойчивой конфигурации инертного газа радона.
- Почему низшие состояния нестабильны? В отличие от лантаноидов, у тория электроны 5f-подуровня не всегда заселены в основном состоянии, и элемент предпочитает сразу переходить в максимально окисленную форму, минуя промежуточные стадии.
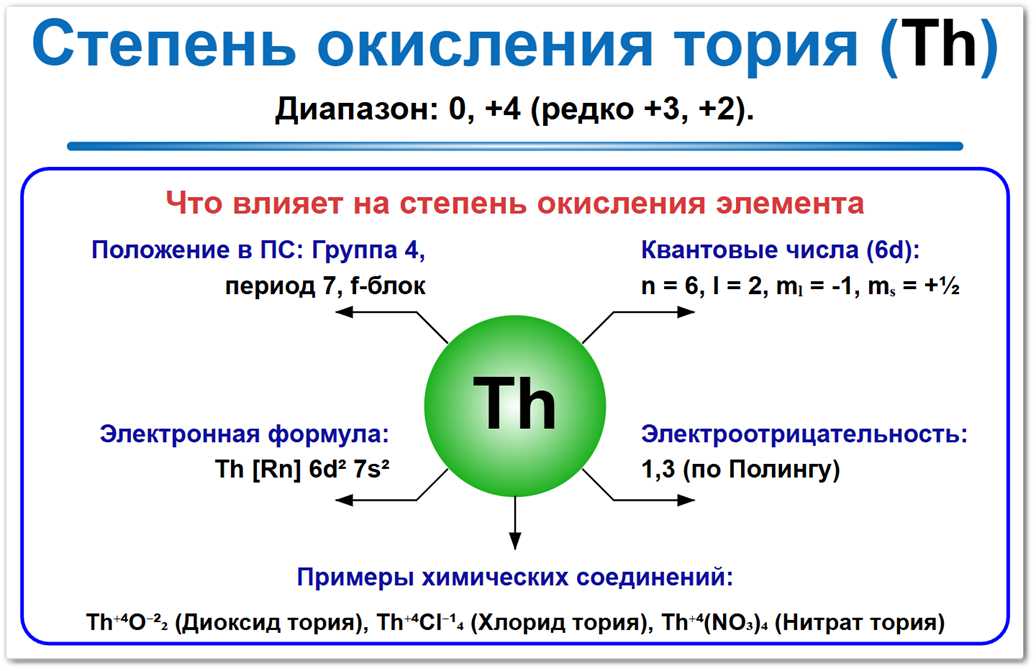
Рис. 1. Возможные степени окисления тория: 0, +2, +3 и +4.
Состояние +4 является единственным устойчивым в водных растворах, где торий образует бесцветные ионы.
Любые попытки получить низшие формы в присутствии воды приводят к их мгновенному окислению до +4 с выделением водорода.
Важно подчеркнуть, что торий является радиоактивным элементом.
Его долгоживущий изотоп Th-232 имеет период полураспада, сопоставимый с возрастом Земли, что делает его важным объектом в ядерной энергетике.
На химическую специфику этого металла влияют электронная структура ([Rn] 6d2 7s2), отсутствие электронов на 5f-орбитали в основном состоянии и электроотрицательность 1,3 по Полингу.
Содержание страницы
- 1. Почему +4 — доминирующая степень окисления у тория
- 2. Степень окисления тория в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему торий отдает 4 электрона?
- 4. 4 способа определить степень окисления тория
- 4.1. По таблице Менделеева
- 4.2. По валентности (Количество связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления тория
- 6. Шпаргалка для тория
- 7. Торий вне учебника: что скрывают редкие состояния?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +4 — доминирующая степень окисления у тория
Причина непоколебимости четырехвалентного состояния заключается в полной ионизации всех доступных внешних электронов, что превращает ион Th⁴⁺ в очень стабильную систему.
- В простом веществе (Th0): Заряд равен 0. Конфигурация:
[Rn] 6d2 7s2. - В четырехзарядном ионе (Th+4): Металл теряет все 4 валентных электрона. Конфигурация:
[Rn](полностью завершенная оболочка).

Рис. 2. Схема образования степени окисления +4: удаление двух 7s и двух 6d-электронов для формирования стабильного катиона Th4+.
Степень окисления тория в соединениях
В зависимости от химического окружения, торий в веществах проявляет степень окисления, которая диктует структуру кристаллической решетки:
- Нитрат тория(IV) (Th(NO3)4): Th +4.
- Диоксид тория (ThO2): Th +4 (самый тугоплавкий оксид).
- Тетрабромид тория (ThBr4): Th +4.
- Оксалат тория(IV) (Th(C2O4)2): Th +4.
- Гидрид тория (ThH2): формально Th +2 (нестехиометрическое соединение).
Высшая степень окисления
Максимальная степень окисления Th составляет +4. В отличие от соседних урана или плутония, торий не способен проявлять состояния +5 или +6.
Так как у него нет достаточного количества электронов на доступных орбиталях.
Низшая степень окисления
Для этого элемента стандартной минимальной степенью является 0 в металлическом виде. Отрицательные значения в классической химии не зафиксированы.
Промежуточные степени окисления
Заряд тория в молекулах крайне редко отклоняется от +4.
Состояния +2 и +3 получены только в составе «кластерных» галогенидов или экзотических комплексов, где атомы металла связаны друг с другом, и они крайне чувствительны к воздуху.
Важно: Торий в степени +4 обладает высоким координационным числом (часто 8 или 9), что позволяет ему образовывать сложнейшие по структуре степень окисления тория формула соединения, важные для радиохимического разделения элементов.
Почему торий отдает 4 электрона?
Характер поведения элемента определен его стартовой позицией в ряду актиноидов:
- Положительный заряд (+): Торий — активный металл, который легко расстается с электронами при контакте с неметаллами.
- Отсутствие отрицательных СО (-): Из-за внушительного радиуса и низкой электроотрицательности торий физически не способен удерживать дополнительные электроны.
4 способа определить степень окисления тория
По таблице Менделеева
- Семейство: f-элемент (формально, хотя электроны часто на d-подуровне).
- Валентные частицы: 4 электрона (6d2 7s2).
- Атомная масса тория: 232,04 а.е.м.
По валентности (Количество связей)
Почти всегда валентность тория равна IV.
- В ThO2: Торий формирует связи, эквивалентные валентности IV, СО — +4.
- В ThF4: Торий связан с четырьмя атомами фтора, СО — +4.
По электронной конфигурации
- Электронная формула тория: [Rn] 6d2 7s2.
- Атому тория степени окисления +4 достичь проще всего, так как это полностью опустошает внешний слой, создавая симметричную электронную систему.
По химическому соединению (Алгебраический расчет)
Пример для Th(SO4)2:
Суммарный заряд равен 0. Сульфат-группа (SO4) имеет заряд -2. Обозначим торий как x.
x + 2 · (-2) = 0 ⇒ x — 4 = 0 ⇒ x = +4
Примеры степеней окисления тория
| СО | Краткое описание | Примеры веществ |
|---|---|---|
| +4 | Постоянная. Единственная форма, устойчивая в природе и быту. | ThO2, ThCl4, Th(NO3)4 |
| +3 / +2 | Экзотическая. Нестабильные формы, существующие в вакууме или аргоне. | ThI3, ThI2, ThS |
| 0 | Металл. Состояние простого вещества, медленно темнеющего на воздухе. | Th (компактный металл) |
Шпаргалка для тория
- +4 — «золотой стандарт» для тория, другие состояния в школе и вузе обычно не изучаются.
- Радиоактивность — торий всегда проявляет слабую природную активность, независимо от СО.
- Тугоплавкость — оксид тория(IV) плавится при 3300°C, что делает его чемпионом среди оксидов.
Торий вне учебника: что скрывают редкие состояния?
+3: Долгое время считалось невозможным, но было получено в составе иодида ThI3.
Это твердое черное вещество, которое мгновенно разлагается при контакте с малейшими следами влаги.
+2: Встречается в так называемых «черных иодидах» тория.
Эти соединения обладают металлической проводимостью, что указывает на то, что электроны не просто сидят на атоме, а частично делокализованы.
Комплексы: Современная химия создала органические молекулы, которые «заставляют» торий удерживать низкие степени окисления, защищая его от окисления громоздкими молекулярными группами.
Пример решения задачи:
▶️ Дано:
Соединение: ThCl4 (тетрахлорид тория).
⌕ Найти:
Определите СО тория.
✨ Решение:
Хлор (Cl) как галоген в бинарных соединениях с металлами всегда имеет заряд -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Th(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: у тория всего 4 валентных электрона, поэтому СО +7 для него физически невозможна.
Часто задаваемые вопросы
Однозначно — состояние +4.
Нет, это электроположительный металл, он только отдает заряды.
Потому что другие состояния (+2, +3) настолько нестабильны, что их невозможно встретить в природе или обычной лаборатории.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.