Теория:
Степень окисления теннессина (Ts) в химических соединениях, согласно теоретическим расчетам, может принимать значения -1, +1, +3 и +5.
Это обусловлено положением элемента в 17-й группе Периодической системы (галогены).
Поэтому из-за сильных релятивистских эффектов его химия значительно отличается от химии иода или астата.
Кроме того, выделяют показатель 0, который относится к теннессину в виде простого вещества.
Например, для предполагаемой СО +3: в гипотетическом соединении TsF3 (трифторид теннессина) заряд иона равен +3.
В отличие от легких галогенов, для теннессина более высокие степени окисления могут быть более стабильными из-за особенностей 7p-подоболочки.
Для сравнения, другие СО: состояние -1 (типичное для галогенов) для теннессина является менее предпочтительным, чем для хлора или брома, так как его электроотрицательность значительно ниже.
- Почему +1 и +3? Электронная конфигурация теннессина [Rn] 5f14 6d10 7s2 7p5 из-за спин-орбитального взаимодействия разделяет 7p-уровень на две подоблочки. Это делает отдачу одного или трех электронов энергетически возможной.
- Почему СО -1 менее вероятна? Огромный заряд ядра и релятивистские эффекты делают теннессин скорее «металлическим» галогеном, которому труднее удерживать лишний электрон.
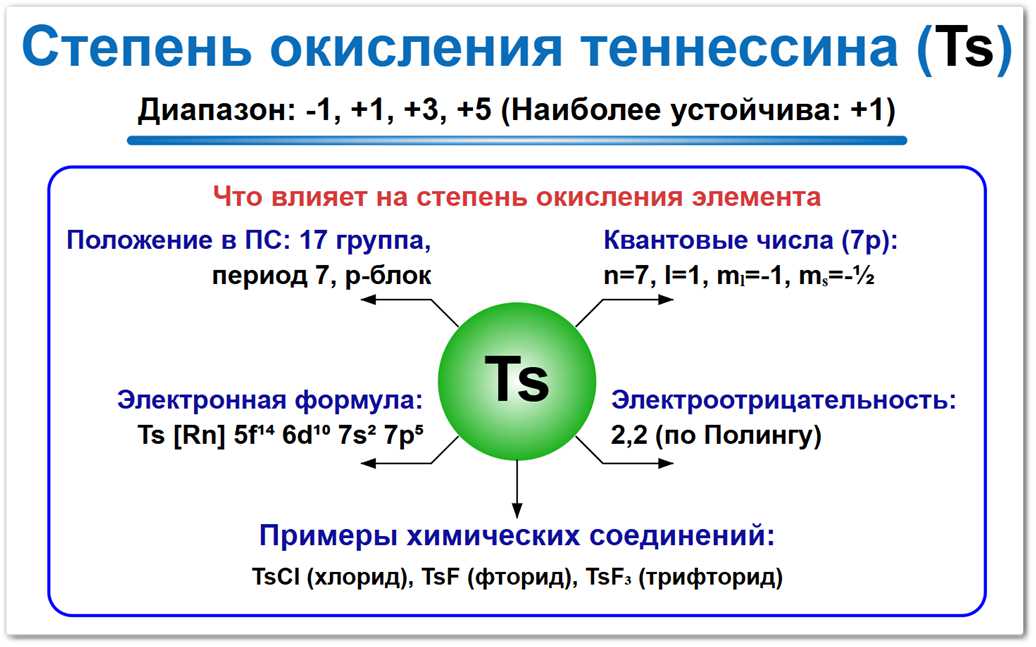
Рис. 1. Основные и прогнозные степени окисления теннессина: 0, -1, +1, +3, +5.
На текущий момент теннессин изучен крайне мало. Эксперименты подтверждают лишь его физическое существование, в то время как химические свойства остаются областью квантовохимического моделирования.
Важно заметить, что теннессин — один из самых тяжелых элементов (117), время жизни его изотопов исчисляется миллисекундами.
Это делает невозможным применение классических методов химии.
Все выводы строятся на экстраполяции свойств группы и сложнейших расчетах поведения 7p-электронов.
Содержание страницы
- 1. Почему степени окисления теннессина так необычны?
- 2. Степень окисления теннессина в соединениях (прогноз)
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему теннессин может иметь заряд +3?
- 4. 4 способа определить степень окисления теннессина
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления теннессина
- 6. Шпаргалка
- 7. Теннессин вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему степени окисления теннессина так необычны?
Стабильность определяется релятивистским разделением p-орбиталей на уровни с разной энергией.
- В простом веществе (Ts0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d10 7s2 7p5. - В высшей степени окисления (Ts+5): Потеря всех пяти 7p-электронов. Конфигурация:
[Rn] 5f14 6d10 7s2.

Рис. 2. Схема образования степеней окисления: отдача электронов с 7p-подоболочек.
Степень окисления теннессина в соединениях (прогноз)
- Теннессид водорода (HTs): Ts -1 (наименее стабилен среди галогеноводородов).
- Монофторид теннессина (TsF): Ts +1.
- Трифторид теннессина (TsF3): Ts +3.
Высшая степень окисления
Высшая степень окисления Ts теоретически равна +5 (в отличие от +7 у легких галогенов, так как 7s2 электроны становятся очень инертными).
Низшая степень окисления
Характерна степень окисления -1, но она проявляется гораздо слабее, чем у иода.
Промежуточные степени окисления
Стабильными считаются +1 и +3, что делает теннессин химически похожим на золото или таллий в некоторых реакциях.
Важно: Теннессин — второй из самых тяжелых известных элементов. Его открытие в 2010 году заполнило предпоследнюю клетку 7-го периода.
Почему теннессин может иметь заряд +3?
- Релятивистские эффекты: Электроны 7p3/2 слабее связаны с ядром, чем 7p1/2, что облегчает их участие в связях.
- Снижение электроотрицательности: В группе галогенов сверху вниз металлические свойства растут, и теннессин — венец этой тенденции.
4 способа определить степень окисления теннессина
По таблице Менделеева
- Семейство: Галогены (формально), трансактиноиды.
- Валентные электроны: 7 (7s2 7p5).
- Атомная масса: ~294 а.е.м.
По валентности (Число связей)
Валентность теннессина (Ts) может быть I, III и V.
В отличие от фтора, который всегда одновалентен, теннессин за счет свободных или легкодоступных подуровней может образовывать несколько связей с сильными окислителями.
По электронной конфигурации
Электронная формула теннессина: [Rn] 5f14 6d10 7s2 7p5.
Механизм ионизации:
- Разделение уровней: 7p-подуровень делится на 7p1/2 (2 электрона) и 7p3/2 (3 электрона).
- СО +3: Атом теряет три электрона с наиболее удаленного уровня 7p3/2.
- СО +5: Теряются все пять 7p-электронов.
По химическому соединению (Алгебраический расчет)
Пример для TsF3:
- 1. Фтор (F) — самый электроотрицательный элемент, СО всегда -1.
- 2. 3 атома фтора дают заряд: 3 · (-1) = -3.
- 3. Уравнение для нейтральной молекулы: x + (-3) = 0.
- 4. Результат: x = +3.
✅ Вывод: Степень окисления теннессина в трифториде равна +3.
Примеры степеней окисления теннессина
| СО | Характеристика | Примеры |
|---|---|---|
| +3, +1 | Наиболее вероятные катионные формы. | TsF3, TsCl |
| -1 | Типичная для галогенов (нестабильна). | HTs, ATs |
Шпаргалка
- +3 — ожидаемая наиболее характерная СО в соединениях с фтором.
- Металлический характер — теннессин ближе к металлам, чем любой другой галоген.
Теннессин вне учебника: что скрывает наука?
Металл или неметалл?
Если бы мы могли собрать миллиард атомов теннессина, он, скорее всего, выглядел бы как блестящий полуметалл, а не как газообразный хлор.
Его температура кипения предсказывается в районе 550°C.
Остров стабильности:
Теннессин находится на пути к так называемому «острову стабильности».
Ученые надеются, что его более тяжелые изотопы смогут жить минуты или даже часы, что позволит провести настоящие химические опыты в пробирке.
Интересный факт: Название дано в честь штата Теннесси (США), где расположены научные центры, внесшие огромный вклад в изучение трансурановых элементов.
Пример решения задачи:
▶️ Дано:
Соединение: TsF (монофторид теннессина).
⌕ Найти:
Определите степень окисления (СО) теннессина.
✨ Решение:
1. Фтор (F) всегда имеет СО -1.
2. Молекула электронейтральна (сумма зарядов = 0).
3. Обозначим СО теннессина за x:
x + (-1) = 0 ⇒ x = +1.
✅ Ответ:
СО теннессина (Ts) в данном соединении равна +1.
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: теннессин самый электроположительный среди галогенов.
Часто задаваемые вопросы
+1, из-за релятивистского упрочнения внутренних оболочек, мешающего электронам участвовать в связях.
Из-за релятивистского эффекта «инертной пары» 7s-электроны сидят слишком глубоко и неохотно участвуют в реакциях, поэтому высшая СО ограничивается +5.
-1 у теннессина теоретически возможна, но она крайне нестабильна и практически не проявляется. Потому, что он слишком тяжелый и «металлический», чтобы вести себя как нормальный галоген.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.