Теория:
Степень окисления лютеция (Lu) в подавляющем большинстве химических соединений принимает фиксированное значение +3.
В отличие от своего соседа иттербия, для этого элемента состояния ниже +3 практически не встречаются в устойчивом виде.
Также не стоит забывать про состояние 0, которое характерно для лютеция в форме простого вещества (металла).
Например для единственно стабильной СО +3: в веществе Lu2O3 (оксид лютеция) заряд металла составляет +3.
Для сравнения: лютеций завершает ряд лантаноидов, и его химическое поведение отличается исключительным постоянством валентных состояний.
- Почему только +3? Это обусловлено строением электронных оболочек: лютеций с готовностью отдает два 6s-электрона и единственный электрон с 5d-подуровня.
- Почему нет +2? У лютеция электронная конфигурация [Xe] 4f14 5d1 6s2. В отличие от иттербия, потеря всего двух электронов не создает дополнительной симметрии, так как остается «лишний» 5d-электрон. Атому выгоднее избавиться от всей внешней группы зарядов.
- Почему невозможна +4? Слой 4f14 у лютеция полностью укомплектован и максимально приближен к ядру (лантаноидное сжатие). Чтобы извлечь из него четвертый электрон, потребовался бы колоссальный энергетический потенциал, недоступный в химических процессах.
Заметим, что химия лютеция в его основном состоянии +3 проявляет значительное сходство с химией иттрия (Y) и скандия (Sc).
Это объясняется идентичностью строения их внешних электронных уровней и близостью химических свойств.
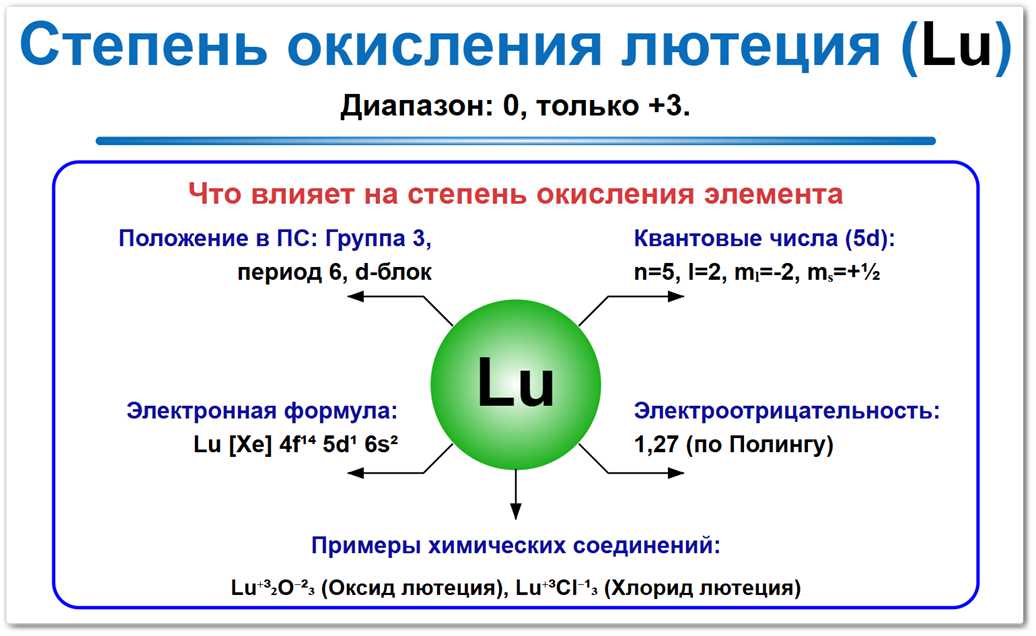
На специфику его реакций воздействуют электронная структура (4f14 5d1 6s2), статус замыкающего элемента в группе лантаноидов и показатель электроотрицательности 1,27 по шкале Полинга.
Содержание страницы
- 1. Почему +3 — самая стабильная степень окисления у лютеция
- 2. Степень окисления лютеция в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему лютеций только отдает электроны?
- 4. Как определить степень окисления лютеция
- 4.1. По периодической таблице
- 4.2. По валентности (Число химических связей)
- 4.3. По электронной формуле
- 4.4. По химической формуле (Расчетный метод)
- 5. Примеры степеней окисления лютеция
- 6. Шпаргалка для лютеция
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 — самая стабильная степень окисления у лютеция
Причина неизменности валентного состояния лютеция кроется в наличии полностью завершенного 4f-подуровня, который остается интактным (нетронутым) при химических превращениях.
- В элементарном веществе (Lu⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d1 6s2. - В катионе (Lu+3): Лютеций лишается 3 электронов. Конфигурация:
[Xe] 4f14(идеально стабильный, заполненный слой).

Рис. 2. Трансформация лютеция: переход от металлической структуры к стабильному катиону +3 в результате потери трех валентных электронов.
Степень окисления лютеция в соединениях
Независимо от агрессивности среды, лютеций в составе веществ проявляет степень окисления, которая гарантирует стабильность кристаллической решетки и отсутствие парамагнитных свойств (в большинстве случаев):
- Оксид лютеция(III) (Lu2O3): Lu +3, O -2.
- Хлорид лютеция(III) (LuCl3): Lu +3, Cl -1.
- Нитрат лютеция (Lu(NO3)3): Lu +3.
- Фосфат лютеция (LuPO4): Lu +3.
- Фторид лютеция(III) (LuF3): Lu +3.
Высшая степень окисления
Высшая степень окисления Lu составляет +3. Дальнейшее повышение заряда невозможно из-за инертности 4f-оболочки.
Низшая степень окисления
В отличие от соседей по ряду, у него нет устойчивой СО +2. Таким образом, минимальная степень окисления лютеция равна 0 в его металлической модификации.
Промежуточные степени окисления
Степень окисления лютеция в молекулах не имеет промежуточных значений.
Элемент демонстрирует редкое для переходных металлов однообразие валентных форм.
Важно: Благодаря стабильности заряда +3 и отсутствию f-f переходов (слой 4f заполнен), соединения лютеция прозрачны и бесцветны, что делает его степень окисления лютеция формула соединения идеальной основой для сцинтилляционных кристаллов в медицине.
Почему лютеций только отдает электроны?
Направление электронного обмена предопределено низкой электроотрицательностью и типично металлическим характером элемента:
- Положительная СО (+): Атом легко расстается с тремя электронами, стремясь к энергетическому минимуму.
- Нулевая СО (0): Свойственна для тяжелого, тугоплавкого металла.
- Отрицательная СО (-): Физически невозможна, так как лютеций является активным металлом-донором.
Как определить степень окисления лютеция
По периодической таблице
- Блок: d-элемент (по формальному строению) или f-элемент (по принадлежности к лантаноидам).
- Валентные орбитали: 6s² и 5d¹.
- Атомная масса лютеция: 175 а.е.м.
По валентности (Число химических связей)
Практически во всех ситуациях валентность лютеция строго равна III.
- В оксиде (Lu2O3): Каждый атом металла формирует по три связи, что соответствует СО +3.
- В гидроксиде (Lu(OH)3): Лютеций удерживает три гидроксильные группы, проявляя валентность III.
По электронной формуле
- Электронная конфигурация лютеция: [Xe] 4f14 5d1 6s2.
- Атому лютеция степени окисления +3 достичь максимально выгодно, так как это полностью очищает уровни 6s и 5d.
Для анализа распределения электронов используй таблицу квантовых чисел.
По химической формуле (Расчетный метод)
Пример для LuF3 (фторид лютеция):
Алгебраическая сумма зарядов — 0. Фтор всегда -1. Ищем Lu (x).
x + 3 · (-1) = 0 ⇒ x = +3
Примеры степеней окисления лютеция
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Единственная устойчивая. Стандарт для всех солей. | Lu2O3, Lu(NO3)3, LuCl3 |
| 0 | Металлическая. Состояние чистого химического элемента. | Lu (слиток, порошок) |
Шпаргалка для лютеция
- +3 — стабильное состояние, не склонное к окислительно-восстановительным переходам.
- Диамагнетизм — из-за СО +3 и заполненного f-слоя ионы лютеция не притягиваются магнитом.
- Чистота — соединения лютеция(III) обычно не имеют окраски.
Пример решения задачи:
▶️ Дано:
Соединение: Lu(NO3)3 (нитрат лютеция).
⌕ Найти:
Вычислите СО лютеция.
✨ Решение:
Нитрат-ион (NO₃) имеет суммарный заряд -1. В формуле их три. Уравнение: x + 3 · (-1) = 0 → x = +3.
✅ Ответ:
Lu(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: в растворах лютеций существует исключительно в виде иона Lu³⁺.
5 — неверно: даже при сильном нагревании лютеций не меняет степень окисления выше +3.
Часто задаваемые вопросы
Безусловно, это степень окисления +3.
Потому что у лютеция есть дополнительный 5d-электрон, который делает состояние +2 энергетически невыгодным по сравнению с полным окислением до +3.
Нет, лютеций — типичный металл, способный только отдавать отрицательные частицы.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.